Анализ крови на сосуды инвитро
Метод определения
См. в описании
Исследуемый материал
Смотрите в описании
Кровь — это жидкая ткань, выполняющая различные функции, в том числе, транспорта кислорода и питательных веществ к органам и тканям и выведения из них шлаковых продуктов. Состоит из плазмы и форменных элементов: эритроцитов, лейкоцитов и тромбоцитов.

Общий анализ крови в лаборатории ИНВИТРО включает в себя определение концентрации гемоглобина, количества эритроцитов, лейкоцитов и тромбоцитов, величины гематокрита и эритроцитарных индексов (MCV, RDW, MCH, MCHC). Общий анализ — см. тест № 5, Лейкоцитарная формула — см. тест № 119, СОЭ — см. тест № 139.
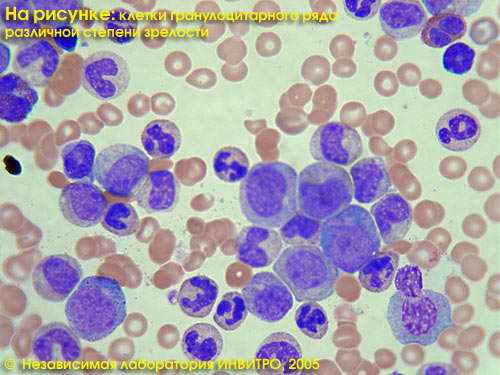
Лейкоцитарная формула — это процентное соотношение различных видов лейкоцитов (нейтрофилы, лимфоциты, эозинофилы, моноциты, базофилы).
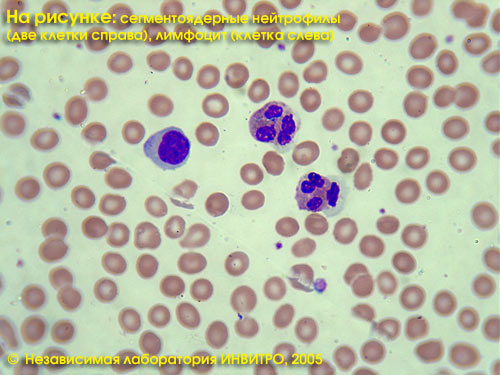
Лейкоцитарная формула в Независимой лаборатории ИНВИТРО включает в себя определение (в %) нейтрофилов, лимфоцитов, эозинофилов, базофилов, моноцитов. Общий анализ — см. тест № 5, Лейкоцитарная формула — см. тест № 119, СОЭ — см. тест № 139.
Скорость оседания эритроцитов (СОЭ) — неспецифический показатель воспаления. СОЭ — показатель скорости разделения крови в пробирке с добавленным антикоагулянтом на 2 слоя: верхний (прозрачная плазма) и нижний (осевшие эритроциты). Скорость оседания эритроцитов оценивается по высоте образовавшегося слоя плазмы (в мм) за 1 час. Удельная масса эритроцитов выше, чем удельная масса плазмы, поэтому в пробирке при наличии антикоагулянта (цитрата натрия) под действием силы тяжести эритроциты оседают на дно.
Процесс оседания (седиментации) эритроцитов можно разделить на 3 фазы, которые происходят с разной скоростью. Сначала эритроциты медленно оседают отдельными клетками. Затем они образуют агрегаты — «монетные столбики», и оседание происходит быстрее. В третьей фазе образуется очень много агрегатов эритроцитов, их оседание сначала замедляется, а потом постепенно прекращается.
Показатель СОЭ меняется в зависимости от множества физиологических и патологических факторов. Значения СОЭ у женщин несколько выше, чем у мужчин. Изменения белкового состава крови при беременности ведут к повышению СОЭ в этот период.
Снижение содержания эритроцитов (анемия) в крови приводит к ускорению СОЭ и, напротив, повышение содержания эритроцитов в крови замедляет скорость седиментации. В течение дня возможно колебание значений, максимальный уровень отмечается в дневное время. Основным фактором, влияющим на образование «монетных столбиков» при оседании эритроцитов является белковый состав плазмы крови. Острофазные белки, адсорбируясь на поверхности эритроцитов, снижают их заряд и отталкивание друг от друга, способствуют образованию «монетных столбиков» и ускоренному оседанию эритроцитов.
Повышение белков острой фазы, например, С-реактивного белка, гаптоглобина, альфа-1-антитрипсина, при остром воспалении приводит к повышению СОЭ. При острых воспалительных и инфекционных процессах изменение скорости оседания эритроцитов отмечается через 24 часа после повышения температуры и увеличения числа лейкоцитов. При хроническом воспалении повышение СОЭ обусловлено увеличением концентрации фибриногена и иммуноглобулинов.
Определение СОЭ в динамике, в комплексе с другими тестами, используют в контроле эффективности лечения воспалительных и инфекционных заболеваний. Общий анализ — см. тест № 5, Лейкоцитарная формула — см. тест № 119, СОЭ — см. тест № 139.
Биоматериал – 2 пробирки:
Цельная кровь с ЭДТА
Цельная кровь с цитратом
Обращаем внимание, что при выполнении клинического анализа крови (
№1515
) и подсчете лейкоцитарной формулы (
№119
), если в пробах выявлены значимые отклонения и результат требует проведения ручной микроскопии, ИНВИТРО дополнительно бесплатно проводит ручной подсчет лейкоцитарной формулы с подсчетом молодых форм нейтрофилов (в том числе точным подсчетом палочкоядерных нейтрофилов) и количественной оценкой всех патологических форм лейкоцитов (при их наличии).
Источник
Показания к назначению:
- обследование лиц старше 18 лет для оценки риска сердечно-сосудистых заболеваний с целью первичной профилактики.
Описание:
Исследование липидного профиля в условиях «не натощак» применяют в рамках обследования для оценки риска сердечно-сосудистых заболеваний с целью первичной профилактики.
Скрининговый комплекс тестов липидного профиля наиболее часто назначается для оценки риска развития сердечно-сосудистых заболеваний в сочетании с другими факторами риска. Кроме того, результаты исследований используют для уточнения диагноза некоторых генетических нарушений липидного обмена, динамического наблюдения за пациентами в ходе проводимой терапии и контроля ее эффективности.
Ранее обязательным требованием подготовки к исследованию липидного профиля было состояние пациента строго натощак после 8-12-часового периода голодания, поскольку это позволяет стандартизировать условия взятия пробы, снизив влияния недавнего приема пищи. В настоящее время, в соответствии с рекомендациями экспертов, требование состояния натощак перед взятием пробы на липидный профиль не во всех ситуациях является обязательным и может зависеть от клинической задачи при назначении исследования (см. табл. 1).
Таблица 1. Зависимость требования состояния натощак 8-12 часов для липидного профиля от клинической задачи при его назначении.
| Клиническая задача при назначении липидного профиля | Условия взятия пробы |
| Оценка исходного риска сердечно-сосудистых заболеваний у пациентов, не получающих лечение, обследуемых с целью первичной профилактики. | Допустимо и натощак, и не натощак |
| Уточнение диагноза метаболического синдрома. | Допустимо и натощак, и не натощак |
| При проведении гиполипидемической терапии для оценки остаточного риска. | Предпочтительно натощак |
| Оценка состояния здоровья пациентов, подверженных риску панкреатита. | Предпочтительно натощак |
| Диагностика гипертриглицеридемии. | Предпочтительно натощак |
| Скрининг и наблюдение за пациентами с семейным анамнезом генетической гиперлипидемии или преждевременного атеросклеротического сердечно-сосудистого заболевания. | Для диагностики генетических видов дислипидемий целесообразно применять расширенное исследование липидного профиля натощак |
Если в назначения врача входят какие-либо другие тесты, требующие обязательного взятия крови натощак (например, определение уровня глюкозы), исследование липидов целесообразно проводить одновременно в тех же условиях. Кроме того, обследование натощак может потребоваться, если:
- полученное не натощак значение триглицеридов превышает 4,5 ммоль/л, или ранее уже была диагностирована гипертриглицеридемия;
- проводится медикаментозное лечение гипертриглицеридемии;
- проводится лечение панкреатита, связанного с гипертриглицеридемией.
В остальных ситуациях при исследовании липидов можно ориентироваться на правила, приведенные в таблице 1.
При выборе варианта скринигового липидного профиля в условиях не натощак для некоторых тестов меняются пороговые значения в информации по интерпретации кардиориска. Поэтому при обращении в лабораторию следует выбрать верный вариант профиля – «натощак» (
№ОБС54
) или «не натощак» (
№ОБС128
).
Следует отметить, что проведение исследований не натощак удобнее для пациента и направляющего врача, поскольку позволяет выполнить взятие крови в день визита, без дополнительного посещения процедурного кабинета в состоянии натощак. Исследование липидного профиля в условиях не натощак с целью оценки сердечно-сосудистых рисков в рамках первичной профилактики, по мнению ряда экспертов, может быть даже более информативным, чем исследование натощак, поскольку в состоянии не натощак человек находится большую часть суток. Допустимость проведения скрининга липидов не натощак утверждена в клинических рекомендациях профессиональных сообществ РФ.
Более подробно об особенностях липидного профиля не натощак можно ознакомиться
здесь
.
Материал для исследования
Сыворотка крови.
Метод определения и единицы измерения
Интерпретация результатов
Информация по интерпретации тестов липидного профиля в состоянии не натощак (в сравнении с состоянием натощак) при оценке сердечно-сосудистых рисков.
| Не натощак | Натощак | |
| №31 Холестерин общий | Желательный уровень: <5 ммоль/л | Идентично |
| №32 Холестерин-ЛПВП | Уровень холестерола ЛПВП >1,0 ммоль/л у мужчин и >1,2 ммоль/л у женщин указывает на низкий риск. | Идентично |
| Холестерин не-ЛПВП | Желательные значения для группы низкого и умеренного риска: <3,9 ммоль/л | Желательные значения для группы низкого и умеренного риска: <3,8 ммоль |
| №33 Холестерин-ЛПНП | Желательные значения для группы низкого и умеренного риска: <3,0 ммоль/л | Идентично |
| №30 Триглицериды | Уровень <2,0 ммоль/л указывает на низкий риск | Уровень <1,7 ммоль/л указывает на низкий риск |
Основная литература
- Бойцов С.А. и соавт. Кардиоваскулярная профилактика 2017. Российские национальные рекомендации. Российский кардиологический журнал. 2018;23(6):118.
- Driver S.L. et al. Fasting or nonfasting lipid measurements: it depends on the question. Journal of the American College of Cardiology. 2016;67(10):1227-1234.
- Langlois M.R. et al. Quantifying atherogenic lipoproteins: current and future challenges in the era of personalized medicine and very low concentrations of LDL cholesterol. A consensus statement from EAS and EFLM. Clinical chemistry. 2018;64(7):1006-1033.
- Langlois M.R. First EAS-EFLM consensus guideline on non-fasting lipid testing and reporting. European Heart Journal. 2016:15.
- Mach F. et al. 2019 ESC/EAS guidelines for the management of dyslipidaemias: Lipid modification to reduce cardiovascular risk. Atherosclerosis. 2019;290:140-205.
- Nordestgaard B.G. A test in context: lipid profile, fasting versus nonfasting. Journal of the American College of Cardiology. 2017;70(13):1637-1646.
- Nordestgaard B.G. et al. Fasting is not routinely required for determination of a lipid profile: clinical and laboratory implications including flagging at desirable concentration cut-points — a joint consensus statement from the European Atherosclerosis Society and European Federation of Clinical Chemistry and Laboratory Medicine. European heart journal. 2016;37(25):1944-1958.
- Trent U.K. Quantifying atherogenic lipoproteins for lipid-lowering strategies: consensus-based recommendations from EAS and EFLM. Clinical chemistry and laboratory medicine. 2019:22.
Источник
Метод определения
Субпопуляции лимфоцитов – иммунофенотипирование (проточная цитофлюориметрия, безотмывочная технология).
Фагоцитарная активность — оценка фагоцитоза бактерий с флюоресцентной меткой.
Циркулирующие иммунные комплексы (ЦИК) — спектрофотометрия.
Иммуноглобулины A, M, G: иммунотурбидиметрия.
Иммуноглобулин E: хемилюминесцентный иммуноанализ.
Исследуемый материал
Цельная кровь с ЭДТА, цельная кровь с гепарином, сыворотка крови
Скрининговая оценка состояния различных звеньев иммунитета, используемая в диагностике первичных и вторичных иммунодефицитов, аутоиммунных, лимфопролиферативных, инфекционных, гематологических заболеваний.
В состав профиля входят следующие показатели:
- Лимфоциты , абсолютное значение
- Субпопуляции лимфоцитов:
- Т-лимфоциты (CD3+)
- Т-хелперы (CD3+CD4+)
- Т-цитотоксические лимфоциты (CD3+CD8+)
- Иммунорегуляторный индекс (CD3+CD4+/CD3+CD8+)
- В-лимфоциты (СD19+)
- ЕК-клетки (CD3-CD16+CD56+)
- Т-ЕК-клетки (CD3+CD16+CD56+)
- Активированные Т-лимфоциты (CD3+HLA-DR+)
- Активированные клетки, не относящиеся к Т-лимфоцитам (В-лимфоциты и активированные ЕК) (CD3-HLA-DR+)
- Т-лимфоцитов (CD3+CD69+)
- В- и ЕК-лимфоцитов (СD3-CD69+)
- Фагоцитоз (гранулоциты)
- Фагоцитоз (моноциты)
- IgG
- IgA
- IgM
- IgE
Основные субпопуляции лимфоцитов:
Т-лимфоциты – лимфоциты, созревание которых происходит в тимусе (отсюда их название). Они контролируют работу В-лимфоцитов, ответственных за образование антител, т. е. за гуморальный иммунный ответ.
Т-хелперы, Th (от англ. to help – помогать) – разновидность Т-лимфоцитов, несут на своей поверхности структуры, способствующие распознаванию антигенов, презентированных вспомогательными клетками, участвуют в регуляции иммунного ответа, вырабатывая различные цитокины.
Цитотоксические Т-клетки — распознают фрагменты антигена, на поверхности клеток-мишеней, ориентируют свои гранулы по направлению к мишени и высвобождают их содержимое в области контакта с ней. При этом некоторые цитокины являются сигналом гибели (по типу апоптоза) для клеток-мишеней.
В-лимфоциты (от лат. «bursa» — сумка по названию сумки Фабрициуса, в которой созревают эти лимфоциты у птиц) проходят развитие в лимфоузлах и других периферических органах лимфоидной системы. На поверхности эти клетки несут иммуноглобулины, функционирующие как рецепторы к антигенам. В ответ на взаимодействие с антигеном В-лимфоциты отвечают делением и дифференциацией в плазматические клетки, вырабатывающие антитела, посредством которых обеспечивается гуморальный иммунитет.
ЕК-клетки (естественные клетки-киллеры) или натуральные киллеры-клетки с естественной, неиммунной цитотоксической активностью к неопластически изменённым клеткам-мишеням, которые не относятся ни к зрелым Т- или В-лимфоцитам, ни к моноцитам.
Т-ЕК-клетки (ЕКТ) – клетки с естественной неиммунной киллерной активностью, имеющие признаки Т-лимфоцитов.
Активированные лимфоциты.
HLA-DR – один из антигенов MHC класса II (major histocompatibility complex — главный комплекс гистосовместимости), участвующих в презентации потенциально чужеродных антигенов, что необходимо для формирования адекватного иммунного ответа. При иммунофенотипировании может быть использован в качестве маркёра активированных клеток. CD3+HLA-DR+ — клетки, представляющие собой зрелые активированные Т-лимфоциты человека. CD3-HLA-DR+ — активированные клетки, не относящиеся к Т-лимфоцитам (В-лимфоциты и активированные ЕК).
Способность лимфоцитов к активации.
Способность лимфоцитов к активации в данном тесте оценивают по содержанию лимфоцитов, экспрессирующих CD69 в ответ на инкубацию в присутствии ФГА (митоген растительного происхождения). CD69 (другие названия — activation inducer molecule, AIM; early activation antigen, EA-1) – ранний маркёр активации, трансмембранный белок типа I. Этот белок вовлечен в ранние механизмы активации Т-клеток, ЕК-клеток, В-клеток, моноцитов и тромбоцитов.
Фагоцитарная активность лейкоцитов.
Данные по фагоцитарной активности нейтрофилов и моноцитов (относительное содержание клеток, фагоцитировавших добавленные к пробе при инкубации меченые флюоресцентной меткой бактерии) позволяют оценить резервные возможности этих клеток по поглощению и перевариванию чужеродных агентов.
Циркулирующие иммунные комплексы общие (ЦИК)
Одновременное присутствие высоких концентраций антигенов и их специфических антител может вести к образованию циркулирующих иммунных комплексов. Иммунные комплексы могут выходить из кровотока в мелких сосудах и откладываться в тканях, например, в гломерулах почек, в лёгких, коже, суставах, стенке сосудов. ЦИК обладают способностью связывать и активировать комплемент, что ведёт к повреждению ткани. Повышение уровня ЦИК может наблюдаться при аутоиммунных заболеваниях, хронических инфекционных заболеваниях, при которых постоянная продукция антигена инфекционным агентом сочетается с иммунным ответом на него (хронические гепатиты). Клинически это часто проявляется гломерулонефритами, артритами, нейропатиями. Несмотря на непосредственную роль в патогенезе некоторых заболеваний, определение ЦИК не всегда информативно, поскольку количество иммунных комплексов, отложившихся в тканях более важно, чем количество комплексов, циркулирующих в крови. Исследование ЦИК может быть недостаточно чувствительным и специфичным в диагностике болезней, вызываемых иммунными комплексами, и должно дополняться исследованием эффектов ЦИК на функцию органов (например, концентрация креатинина и анализ мочи), а также определением С3 С4 компонентов комплемента (см. тест
№ 193
), количество которых снижается вследствие усиленного потребления.
Данные иммунологического исследования интерпретирует врач-иммунолог в комплексе со всеми клинико-анамнестическими данными конкретного пациента. При оценке иммунного статуса пациента результаты исследования оценивают с точки зрения природы и стадии патологического процесса, сопутствующих заболеваний, приёма лекарственных препаратов и пр. При этом важны не только абсолютные значения отдельных показателей, но и их соотношение и динамика показателей. Изменения иммунологических показателей могут быть проявлением нормальной реакции организма на воздействие физиологических или патологических факторов (с различной картиной сдвигов на разных стадиях заболевания), отражать чрезмерную активацию, истощение иммунной системы, характеризовать врождённый или приобретённый дефект отдельных звеньев иммунной системы.
Литература
- Зурочка А.В., Хайдуков С.В. и др. — Проточная цитометрия в медицине и биологии. – Екатеринбург: РИО УрО РАН, 2013. – 552 с.
- Клиническая иммунология и аллергология / Ред. Лолор-младший Г., Фишер Т, Д. Адельман Д../: Пер. с англ. — М.: Практика, 2000. — 806 с.
- Клиническая лабораторная диагностика. Национальное руководство. Том 2./Ред. Долгов В.В., Меньшиков В.В./ – М., ГЭОТАР-Медиа, 2012 – 808 с.
- Практическое руководство по детским болезням. Том 8 Иммунология детского возраста. /Ред. А.Ю.Щербина, Е.Д.Пашанов/ — Москва: МЕДПРАКТИКА, 2006 — 432 с.
- Ройт А., Бростофф Д., Дейл Д. Иммунология. — М.: Мир, 2000 — 592 с
- Ярилин А. А. Иммунология. – М.: ГЭОТАР-Медиа. 2010 — 752 с.
- Leach М., Drummond М., Doig A. Practical Flow Cytometry in Haematology Diagnosis Hardcover. – WILEY-BLACKWELL, 2013.
- Tietz Clinical guide to laboratory tests. 4-th ed. Ed. Wu A.N.B. – USA: W.B Sounders Company, 2006 — 1798 p.
Источник
Метод определения
Твердофазный иммуноферментный анализ (ИФА)
Варианты применяемых тест-систем и их регистрационные удостоверения:
Исследуемый материал
Сыворотка крови
Пожалуйста, заполните
анкету
, это ускорит время приема в медицинском центре. Просим вас также заранее распечатать и заполнить анкету (
Анкета-опросник для пациента.pdf
) при вызове службы «Выезда на дом», это сэкономит ваше время на оформление документов. При себе необходимо иметь документ, удостоверяющий личность (паспорт или иной установленный законодательством документ).
Определение специфических антител класса IgG к коронавирусу SARS-CoV-2 – возбудителю тяжелого острого респираторного синдрома (COVID-19).
Новый коронавирус SARS-CoV-2 относится к семейству РНК-содержащих вирусов семейства Coronaviridae, линии Beta-CoV B.
Основным источником инфекции является больной человек, в том числе находящийся в инкубационном периоде заболевания.
Передача инфекции осуществляется воздушно-капельным, воздушно-пылевым и контактным путями. Ведущим путем передачи SARS-CoV-2 является воздушно-капельный, который реализуется при кашле, чихании и разговоре на близком (менее 2 метров) расстоянии. Контактный путь передачи осуществляется во время рукопожатий и при других видах непосредственного контакта с инфицированным человеком, а также через пищевые продукты, поверхности и предметы, контаминированные вирусом.
Инкубационный период составляет от 2 до 14 суток, в среднем 5-7 суток.
Диагноз устанавливается на основании клинического обследования, данных эпидемиологического анамнеза, результатов инструментальных и лабораторных исследований.
Наиболее частыми клиническими симптомами данной инфекции являются: повышение температуры тела, кашель (сухой или с небольшим количеством мокроты), одышка, утомляемость, ощущение заложенности в грудной клетке.
Рекомендованным методом специфической лабораторной диагностики является выявление РНК SARS-CoV-2 методом ПЦР.
Иммуноглобулины G начинают вырабатываться в организме через 21-28 дней после контакта с вирусом, их уровень увеличивается медленно, но долгое время может оставаться высоким – иногда несколько лет. По наличию и уровню IgG антител в крови можно судить о факте инфицирования в прошлом и определить наличие специфического иммунного ответа – способности организма распознавать вирус при повторной встрече с ним.
Литература
- Лабораторное тестирование случаев, подозреваемых на коронавирусную инфекцию (COVID-19). Временное руководство 19 марта 2020 г. ВОЗ. Европейское региональное бюро.
- Временные методические рекомендации. Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19). Версия 6 (28.04.2020).
- Guo L. et al. Profiling Early Humoral Response to Diagnose Novel Coronavirus Disease (COVID-19). Clin Infect Dis. 2020;ciaa310. doi: 10.1093/cid/ciaa310
- Sethuraman N., Jeremiah S., Ryo A. Interpreting Diagnostic Tests for SARS-CoV-2. JAMA. Published online May 6, 2020:Е1-Е3. doi:10.1001/jama.2020.8259
- Interpretación de las pruebas diagnósticas frente а SARS-CoV-2. 24 de abril de 2020. versión 2. Colaboración Sociedad española de Enfermedades Infecciosas y Microbiología Clínica (SEIMC)
Пожалуйста, заполните
анкету
, это ускорит время приема в медицинском центре. Просим вас также заранее распечатать и заполнить анкету (
Анкета-опросник для пациента.pdf
) при вызове службы «Выезда на дом», это сэкономит ваше время на оформление документов. При себе необходимо иметь документ, удостоверяющий личность (паспорт или иной установленный законодательством документ).
Специальной подготовки не требуется. Рекомендуется взятие крови не ранее чем через 4 часа после последнего приема пищи.
- в целях уточняющей диагностики COVID-19, в дополнение к ПЦР-тестам;
- для оценки предполагаемого иммунного статуса пациента.
Пожалуйста, заполните
анкету
, это ускорит время приема в медицинском центре. Просим вас также заранее распечатать и заполнить анкету (
Анкета-опросник для пациента.pdf
) при вызове службы «Выезда на дом», это сэкономит ваше время на оформление документов. При себе необходимо иметь документ, удостоверяющий личность (паспорт или иной установленный законодательством документ).
Интерпретация результатов
Интерпретация результатов исследований содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Пожалуйста, заполните
анкету
, это ускорит время приема в медицинском центре. Просим вас также заранее распечатать и заполнить анкету (
Анкета-опросник для пациента.pdf
) при вызове службы «Выезда на дом», это сэкономит ваше время на оформление документов. При себе необходимо иметь документ, удостоверяющий личность (паспорт или иной установленный законодательством документ).
Единицы измерения
Тест качественный. Результаты выдаются в терминах «положительно», «отрицательно», «сомнительно».
Интерпретация результатов
При положительном результате выдается значение коэффициента позитивности.*
«Положительно»: инфекция SARS-CoV-2 (текущая или имевшая место в прошлом).
«Отрицательно»:
- ранний период инфекции;
- отсутствие инфекции;
- выздоровление (отдаленные сроки).
«Сомнительно»: пограничное значение, которое не позволяет достоверно (с вероятностью более 95%) отнести результат к «положительно» или «отрицательно». Следует учитывать, что такой результат возможен при очень низком уровне антител, который может иметь место, в частности, в начальный период заболевания. В зависимости от клинической ситуации может быть полезным повторное исследование уровня антител через 10-14 дней для оценки динамики.
* Коэффициент позитивности (КП) – это отношение оптической плотности пробы пациента к пороговому значению. КП – коэффициент позитивности является универсальным показателем, применяемым в качественных иммуноферментных тестах. КП характеризует степень позитивности исследуемой пробы и может быть полезен врачу для правильной интерпретации полученного результата. Поскольку коэффициент позитивности не коррелирует линейно с концентрацией антител в пробе, не рекомендуется использовать КП для динамического наблюдения за пациентами, в том числе контроля эффективности лечения.
Артикул:
1642
Срок исполнения:
до 5 рабочих дней ?
Указанный срок не включает день взятия биоматериала
Цена:
950 руб
Взятие крови из вены:
- + 220 руб
В этом разделе вы можете узнать, сколько стоит выполнение данного исследования в вашем городе, ознакомиться с описанием теста и таблицей интерпретации результатов. Выбирая, где сдать анализ «Антитела к коронавирусу SARS-CoV-2, IgG (anti-SARS-CoV-2, IgG)» в Москве и других городах России, не забывайте, что цена анализа, стоимость процедуры взятия биоматериала, методы и сроки выполнения исследований в региональных медицинских офисах могут отличаться.
Источник


