Стоимость анализа крови на патологию плода
Метод определения
ПЦР с детекцией в режиме реального времени.
Исследуемый материал
Плазма крови (ЭДТА)
Обнаружение фрагмента Y-хромосомы плода в крови беременной методом полимеразной цепной реакции (ПЦР) с детекцией в режиме реального времени, с целью определение пола плода.
В акушерско-гинекологической практике часто возникает необходимость определения генотипа плода на ранних сроках беременности. До недавнего времени материал для таких исследований получали инвазивно, при хорион- и плацентобиопсиии в ходе амнио- и кордоцентеза. Риск самопроизвольного прерывания беременности в этом случае составляет 2-3%. Открытие наличия фетальных ДНК и РНК в материнской крови послужило основой для развития неинвазивной пренатальной диагностики, которая в отличие от упоминаемых методов, не представляет угрозы течению беременности, т. к. материалом для исследования служит кровь матери. Фетальные клетки, т. е. клетки плода, обнаруживаются в крови женщины, их количество возрастает с увеличением срока беременности, зависит от состояния плаценты и особенностей течения беременности. Выяснение пола плода в первом – начале второго триместра может предотвратить случаи рождения больных детей в семьях с отягощенной наследственностью. Возможно прерывание беременности по медицинским показаниям при наличии у родителей носительства генов заболеваний, сцепленных с полом (например, гемофилии или прогрессирующей мышечной дистрофии Дюшенна/Беккера у матери). Вопрос о прерывании беременности и неблагоприятном прогнозе для жизни плода должен решаться индивидуально перинатальным консилиумом врачей.
Также врачу важно знать пол плода для принятия решения о возможности гормональной терапии беременной в случае наличия у пациентки гиперандрогении надпочечникового генеза (врожденная дисплазия коры надпочечников, ВДКН) или других маскулинизирующих эндокринных заболеваний.
Основным методом пренатального установления пола будущего ребенка является ультразвуковая диагностика, однако на ранних сроках беременности УЗИ не имеет необходимой точности и часто субъективно.
Лабораторный тест, выполняемый для определения пола плода, направлен на обнаружение в крови беременной мультикопийного фрагмента Y хромосомы плода* методом ПЦР в режиме реального времени, что с высокой достоверностью свидетельствует о беременности плодом мужского пола.
Метод, включающий исследование ДНК плода в крови матери, обладает рядом преимуществ:
- относится к неинвазивным для плода процедурам, не несет угрозы течению беременности и не вызывает осложнений;
- исследование фетДНК возможно проводить, начиная со срока 10 акушерских недель беременности;
- точность результата составляет 96-100% и зависит от количества ДНК плода, обнаруживаемой в материнской плазме. **
Аналитические показатели метода
Определяемый участок ДНК – мультикопийный фрагмент Y-хромосомы.
Диагностическая чувствительность: 92-100%.
Диагностическая специфичность: 90-100%.
Чувствительность метода составляет 150 копий геномной ДНК (суммарной ДНК матери и плода) в 1,0 мл исследуемого образца плазмы крови.
*Пол определяется парой половых хромосом: у женщин – ХХ, у мужчин – XY.
** Величина обусловлена состоянием плаценты, особенностью течения беременности и возрастает с увеличением срока беременности.
Литература
- Инструкция по применению набора реагентов для выявления фрагмента Y хромосомы плода в крови матери методом ПЦР в режиме реального времени. Пол плода. ДНК-технология». Регистрационное удостоверение № РЗН 2017/6242.
- Избранные клинические рекомендации по неонатологии. Под ред. Е.Н. Байбариной, Д.Н. Дегтярева. — М.: Изд. «ГЕОТАР-Медиа». 2016. 237.
- Ресурс для специалистов в области молекулярной биологии и клинической диагностики: https://www.dna-technology.ru/information..
Источник
 Пройдите диагностику хромосомных мутаций на основе анализа крови. Исследование входит в программу комплексного скрининга беременных и позволяет рассчитать риск рождения неполноценного ребёнка с точностью до 98%.
Пройдите диагностику хромосомных мутаций на основе анализа крови. Исследование входит в программу комплексного скрининга беременных и позволяет рассчитать риск рождения неполноценного ребёнка с точностью до 98%.
Есть мнение, что хромосомные перестройки в генетическом коде ребёнка возникают только на фоне «плохой» наследственности. Однако научно доказано, что риск мертворождения, самоабортирования, рождения малыша с физическими и умственными отклонениями есть и у здоровых пациенток. Поэтому приказом № 572 МЗ РФ от «01» ноября 2012 г. прохождение анализов на хромосомные мутации рекомендовано всем беременным женщинам.
Стоимость диагностики патологий хромосом
600 Р
Альфа-фетопротеин (АФП) крови
700 Р
Клинический анализ крови
800 Р
Клинический анализ крови CITO
600 Р
Β-ХГЧ
800 Р
В-ХГЧ сito
600 Р
РАРР-А
300 Р
Забор крови
Зачем сдавать анализ на хромосомные патологии плода
Анализ позволяет распознать генные мутации до того момента, когда можно будет прервать беременность без вреда для здоровья женщины. Механизм, который запускает хромосомные перестройки и приводит к аномалиям типа синдром Дауна, Патау, Тёрнера, Эдвардса, до конца не изучен. Поэтому предпосылки к аномалиям развития плода должны быть выявлены как можно раньше.
В нашем центре в рамках пренатального скрининга помимо биохимического анализа крови может быть сделан неинвазивный тест (НИПТ), Natera (USA), информативный уже на 9 неделе беременности.
Отказ от обследования или несвоевременно проведённый генетический анализ не позволят предупредить рождение неполноценного ребёнка.
Специалисты
акушер-гинеколог, гемостазиолог, доктор медицинских наук

акушер-гинеколог, гематолог, гемостазиолог, кандидат медицинских наук
Подготовка и проведение
Оптимальный срок сдачи анализа на хромосомные патологии – 12 неделя, так как в это время наиболее выраженно проявляются признаки генетических аномалий. Кровь исследуется только после получения результатов УЗИ, в противном случае трактовка результатов будет ошибочной.
Анализ венозной крови (материал забирают на голодный желудок) покажет уровень АФП, ХГЧ, РАРР- А – веществ, которые продуцируются плодом и плацентой. По маркерам крови оценивается картина развития эмбриона, исследуется морфология (строение) ДНК, выявляются лишние или повреждённые хромосомы.
Расшифровка и расчет рисков
По результатам УЗИ расчёт рисков осуществляется, исходя из количества маркеров, обнаруженных одновременно. При обнаружении 1 маркера, например, недоразвития носовых костей, прогноз риска хромосомной патологии составляет 2%, а при сочетании 8 и более маркеров – 92%.
При расшифровке маркеров крови любые отклонения от нормативных показателей трактуются как признаки генных мутаций. На сроке 12 недель они должны быть следующими:
| АФП | ХГЧ | РАРР- А |
|---|---|---|
| 0,5-15 МЕ/мл | 13,4-128,5 нг/моль | 0,46-3,73 мЕд/мл |
Недостаток белка АФП указывает на развитие аутоиммунной реакции – организм матери отвергает плод. Такое состояние чревато выкидышем и гибелью плода.
Пониженный уровень ХГЧ свидетельствует о задержке развития плода, плацентарной недостаточности. Повышение показателей позволяет предположить риск синдрома Дауна, хориокарциномы, пузырного заноса.
Низкий уровень РАРР- А говорит о недоразвитии плаценты, больших размерах плода.
Как правило, все показатели изучаются в совокупности, со «ссылкой» на результаты УЗИ.
Куда обратиться в Москве
Медицинский женский центр – единственная клиника в Москве, где работает уникальная лаборатория крови. У нас проводятся не только общеклинические исследования, но и все возможные анализы на патологии гемостаза и хромосомной структуры.
Источник
Неинвазивный пренатальный тест или НИПТ позволяет на раннем сроке беременности выявить у плода самые распространённые генетические заболевания, а также определить пол будущего ребёнка
У человека 23 пары хромосом, которые представляют собой скрученные цепи ДНК, несущие генетическую информацию. Изменения количества некоторых хромосом способны приводить к рождению детей с генетическими заболеваниями. Сегодня их насчитывается более 6500.
Многие из генетических патологий сцеплены с полом — наследуются по половому признаку. В таких случаях определение пола ребёнка проводится по медицинским показаниям.
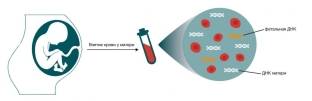
НИПТ предполагает выделение из крови беременной женщины ДНК плода и её последующий анализ с целью выявить наличие распространённых хромосомных синдромов. Метод появился в Европе около 20 лет назад, что ознаменовало начало новой эры эффективных методов определения генетических дефектов плода – без вмешательства в органы и ткани. Prenetix – это один из видов неинвазивной диагностики хромосомных патологий плода.
Цель исследования:
— определить наличие у плода патологии хромосом 21, 18, 13, а также наличие дополнительных хромосом X и Y
— определить пол малыша
Срок проведения: на полной десятой неделе беременности
Подготовка: не требуется, для проведения достаточно 20 миллилитров венозной крови
Получение результатов: в течение 12 рабочих дней
Точность: 99,9%
Безопасность: 100%-ная для здоровья женщины и ребенка. Кровь для анализа забирают из вены, поэтому нет риска выкидыша или занесения инфекции, как в случае инвазивной диагностики. Всемирная Организация Здравоохранения рекомендует его каждой беременной.
Доступность: теперь Prenetix можно пройти в Калининграде, в клинике репродукции «Геном»
В клинике «Геном-Калининград» пройти тест Prenetix может любая беременная женщина, которая хочет получить достоверную информацию о здоровье будущего малыша, а также узнать его пол.
Особенности теста Prenetix:
— показывает точный результат при двуплодной беременности, суррогатном материнстве, беременности, полученной в результате ЭКО, в т.ч. с применением донорских яйцеклеток или сперматозоидов.
— покажет точный пол ребенка с десяти недель, в том числе при двуплодной беременности. На УЗИ половые признаки заметны не ранее 23 недели.
Prenetix — достойная альтернатива классическому скринингу I триместра. В некоторых случаях он позволяет избежать ненужных инвазивных методов диагностики.
Обычное скрининговое обследование в I триместре включает:
— УЗИ плода. Помогает обнаружить отклонения в телосложении и анатомии будущего ребенка, оценить состояние плаценты, пуповины, матки, количество околоплодных вод.
— Двойной тест (биохимический анализ крови). С его помощью определяют уровень связанного с беременностью белка плазмы (РАРР-А) и хорионического гонадотропина (β-ХГЧ). При патологиях плода уровни этих веществ изменяются.
Минус данного исследования — высокий процент ложноположительных результатов, что является показанием для проведения инвазивных исследований. Инвазивные методы предполагают получение биологического материала для лабораторного исследования путём проникновения в матку посредством пункции (прокола). Инвазивные методы часто сопровождаются осложнениями и могут спровоцировать выкидыш. Состояние женщины в период ожидания инвазивного исследования и во время его проведения обычно стрессовое, что крайне нежелательно.
Prenetix определяет наличие следующих патологий:
— Синдром Дауна. Тяжелая умственная отсталость и врождённые пороки. Самая распространённая хромосомная патология.
— Синдром Эдвардса. Олигофрения: патологии черепа, мозга, грудной клетки, сердца. До 5% новорожденных с синдромом Эдвардса доживают до года.
— Синдром Патау. Тяжелые пороки развития, из 100 детей до года доживают 5.
— Синдром Клайнфельтера. Мужское заболевание: патологии эндокринной системы, бесплодие, импотенция.
— Синдром Тёрнера. Женское заболевание: бесплодие, физическая отсталость, склонность к ожирению и сердечным болезням.
— Дополнительные Х и Y хромосомы. Небольшие отклонения в психическом и/или физическом развитии.
Prenetix может показать ложный результат в следующих случаях:
— Беременность более, чем двумя плодами;
— Срок проведения исследования менее двух недель;
— Гибель одного из близнецов.
Prenetix показан в следующих случаях:
— «плохой» результат первого скрининга;
— наличие в анамнезе беременностей с хромосомными мутациями плода;
— поздний репродуктивный возраст будущих родителей (матери от 35 лет, отца от 42 лет);
— выявлены хромосомные нарушения у будущих родителей.
К сведению: Риск появления генетических нарушений у плода увеличивается с возрастом, но он не исключён и в период до 35 лет. По закону врач обязан проинформировать женщину старше тридцати пяти лет о возможности проведения внутриутробного скрининг-теста для выявления пороков развития ребенка.
За последние 25 лет количество женщин, ставших мамами в возрасте старше 35 лет, выросло на 90%. Если еще пятнадцать лет назад неприятным словом «старородящая» называли двадцатипятилетних рожениц, то сегодня «поздний» возраст сдвинулся к 35.
Специалисты клиники «Геном» в Калининграде обладают внушительным опытом ведения беременности, включая сложные случаи. Мы будем рады помочь каждой женщине благополучно пройти период беременности и стать счастливой мамой здорового ребёнка.
Источник
Метод определения
Полимеразная цепная реакция (ПЦР) в режиме реального времени.
Исследуемый материал
Плазма крови (ЭДТА)
Обнаружение гена RHD плода в крови беременной женщины с отрицательным резус-фактором применяют с целью прогнозирования риска развития резус-конфликта и гемолитической болезни плода и новорожденного.
Резус (Rh) – одна из важнейших систем эритроцитарных антигенов (наряду с системой АВ0), клинически значимая при оценке возможности возникновения резус-конфликта и риска развития гемолитической болезни плода и новорожденного.
В системе резус различают пять антигенов. Наиболее иммуногенным является антиген D, аминокислотная последовательность которого кодируется геном RHD. Присутствие антигена D на поверхности эритроцитов определяет положительный резус-фактор (Rh+). Доля резус-положительных лиц, носителей антигена D, в популяции составляет около 86%, а резус-отрицательных лиц (Rh-), не имеющих антигена D – около 14%.
Течение беременности резус-положительным плодом у резус-отрицательных женщин* часто осложняется развитием гемолитической болезни плода, связанной с трансплацентарным переносом эритроцитов плода в кровоток матери. 98% случаев гемолитической болезни новорожденных связаны с D-резус-антигеном. Попадая в кровь резус-отрицательной матери, он вызывает образование специфических антител, которые проникают через плаценту и разрушают эритроциты плода. Это влечет за собой развитие гемолитической болезни плода и новорожденного. При раннем проявлении резус-конфликт может послужить причиной самопроизвольного прерывания беременности или преждевременных родов. Сенсибилизация матери к D-антигену и риск развития резус-конфликта возрастают с каждой последующей беременностью резус-положительным плодом независимо от того, прервалась ли беременность или завершилась родоразрешением.
В настоящее время при выявлении резус-конфликта назначают следующий комплекс исследований:
- измерение уровня специфичных антител матери к D-антигену плода;
- получение плодного материала при хорион- и плацентобиопсии в ходе амнио- и кордоцентеза, что относится к инвазивным методам;
- допплерометрическое исследование скорости кровотока в аорте и средней мозговой артерии плода.
Риск самопроизвольного прерывания беременности при применении инвазивных методов исследования составляет 2-3%, а отсутствие антител не гарантирует, что плод резус-отрицательный, т. к. даже при положительном резусе у плода антитела у матери могут не вырабатываться по причине целостности плаценты в момент обследования или слабого иммунного ответа. Ситуация осложняется тем, что резус-конфликт может возникнуть на любом сроке беременности. Кроме того, возможна сенсибилизация матери. Выявление ДНК плода (фетальной фракции, свободно циркулирующей ДНК, фетДНК) в крови матери обладает рядом преимуществ:
- относится к неинвазивным для плода процедурам, не несет угрозы течению беременности, не вызывает осложнений;
- исследование фетДНК возможно, начиная со срока 10 акушерских недель беременности;
- точность результата 96 – 100%**
- позволяет оценить целесообразность назначения терапии иммуноглобулином при отсутствии в крови беременной женщины анти-резусных антител на сроке 20 недель.
Аналитические показатели метода
Определяемые участки ДНК: 7-й и 10-й экзоны гена RHD. Диагностическая чувствительность: 92-100%. Диагностическая специфичность: 90-100%. Чувствительность метода составляет 150 копий геномной ДНК (суммарной ДНК матери и плода), что соответствует 400 копиям гена RHD плода в 1,0 мл исследуемого образца плазмы.
Ограничения метода
У 1% серологически резус-отрицательных женщин определяется наличие гена RHD. Это происходит в следующих случаях:
- Ген RHD присутствует и генотипически резус-фактор будет положительным, но в результате мутаций D-антиген не синтезируется и серологическим методом определяется как отрицательный;
- Ген RHD присутствует полностью или частично, и генотипически резус-фактор будет положительным; из-за мутаций синтезируется измененный D-антиген. Серологически это определяется или как слабый резус-фактор, или как нестабильно положительный.
По крови таких пациенток определить резус-фактор плода методом ПЦР невозможно. Чаще всего отрицательный резус-фактор обусловлен полным отсутствием гена RHD. В таких случаях применяют серологический метод вместе с ПЦР. Резус-фактор определяется как отрицательный при совпадении отрицательных результатов тестов.
* У беременных женщин, имеющих резус-положительную принадлежность, проблем совместимости по резус-фактору с плодом не возникает.
** Величина обусловлена состоянием плаценты, особенностью течения беременности и возрастает с увеличением срока беременности.
Обращаем внимание, что сроки выполнения ПЦР-исследований могут быть увеличены при проведении подтверждающих тестов.
Противопоказания к проведению исследования:
- Трансплантации органов и тканей в анамнезе у пациентки
Литература
- Costa J.M., Giovangrandi Y., Ernault P., Lohmann L., Nataf V., El Halali N., Gautier E. Fetal RHD genotyping in maternal serum during the first trimester of pregnancy. British journal of haematology. 2002;119:255-260.
- Finning K.M., Martin P.G., Soothill P.W., Avent N.D. Prediction of fetal D status from maternal plasma: introduction of a new noninvasive fetal RHD genotyping service. Transfusion. 2002;42:1079-1085.
- Freeman K., Osipenko L., Clay D., Hyde J., Szczepura A. A Review of Evidence on Non-invasive Prenatal Diagnosis (NIPD): Tests for Fetal RHD Genotype. Workpackage 6, SAFE Network of Excellence Warwick Medical School, UK. 2006.
- Wagner F.F., Frohmajer A., Flegel W.A. RHD positive haplotypes in D negative Europeans. BioMed Central genetics. 2001;15:10.
- Минеева П.В. Группы крови человека. Основы иммуногематологии. – СПб. 2004:188.
- Инструкция по применению набора реагентов для выявления гена RHD плода в крови матери методом ПЦР в режиме реального времени Резус-фактор плода ООО «ДНК-технология». Регистрационное удостоверение № ФСР 2017/5310.
Источник


