Иммунохимический анализ крови и мочи в инвитро
Метод определения
Субпопуляции лимфоцитов – иммунофенотипирование (проточная цитофлюориметрия, безотмывочная технология).
Фагоцитарная активность — оценка фагоцитоза бактерий с флюоресцентной меткой.
Циркулирующие иммунные комплексы (ЦИК) — спектрофотометрия.
Иммуноглобулины A, M, G: иммунотурбидиметрия.
Иммуноглобулин E: хемилюминесцентный иммуноанализ.
Исследуемый материал
Цельная кровь с ЭДТА, цельная кровь с гепарином, сыворотка крови
Скрининговая оценка состояния различных звеньев иммунитета, используемая в диагностике первичных и вторичных иммунодефицитов, аутоиммунных, лимфопролиферативных, инфекционных, гематологических заболеваний.
В состав профиля входят следующие показатели:
- Лимфоциты , абсолютное значение
- Субпопуляции лимфоцитов:
- Т-лимфоциты (CD3+)
- Т-хелперы (CD3+CD4+)
- Т-цитотоксические лимфоциты (CD3+CD8+)
- Иммунорегуляторный индекс (CD3+CD4+/CD3+CD8+)
- В-лимфоциты (СD19+)
- ЕК-клетки (CD3-CD16+CD56+)
- Т-ЕК-клетки (CD3+CD16+CD56+)
- Активированные Т-лимфоциты (CD3+HLA-DR+)
- Активированные клетки, не относящиеся к Т-лимфоцитам (В-лимфоциты и активированные ЕК) (CD3-HLA-DR+)
- Т-лимфоцитов (CD3+CD69+)
- В- и ЕК-лимфоцитов (СD3-CD69+)
- Фагоцитоз (гранулоциты)
- Фагоцитоз (моноциты)
- IgG
- IgA
- IgM
- IgE
Основные субпопуляции лимфоцитов:
Т-лимфоциты – лимфоциты, созревание которых происходит в тимусе (отсюда их название). Они контролируют работу В-лимфоцитов, ответственных за образование антител, т. е. за гуморальный иммунный ответ.
Т-хелперы, Th (от англ. to help – помогать) – разновидность Т-лимфоцитов, несут на своей поверхности структуры, способствующие распознаванию антигенов, презентированных вспомогательными клетками, участвуют в регуляции иммунного ответа, вырабатывая различные цитокины.
Цитотоксические Т-клетки — распознают фрагменты антигена, на поверхности клеток-мишеней, ориентируют свои гранулы по направлению к мишени и высвобождают их содержимое в области контакта с ней. При этом некоторые цитокины являются сигналом гибели (по типу апоптоза) для клеток-мишеней.
В-лимфоциты (от лат. «bursa» — сумка по названию сумки Фабрициуса, в которой созревают эти лимфоциты у птиц) проходят развитие в лимфоузлах и других периферических органах лимфоидной системы. На поверхности эти клетки несут иммуноглобулины, функционирующие как рецепторы к антигенам. В ответ на взаимодействие с антигеном В-лимфоциты отвечают делением и дифференциацией в плазматические клетки, вырабатывающие антитела, посредством которых обеспечивается гуморальный иммунитет.
ЕК-клетки (естественные клетки-киллеры) или натуральные киллеры-клетки с естественной, неиммунной цитотоксической активностью к неопластически изменённым клеткам-мишеням, которые не относятся ни к зрелым Т- или В-лимфоцитам, ни к моноцитам.
Т-ЕК-клетки (ЕКТ) – клетки с естественной неиммунной киллерной активностью, имеющие признаки Т-лимфоцитов.
Активированные лимфоциты.
HLA-DR – один из антигенов MHC класса II (major histocompatibility complex — главный комплекс гистосовместимости), участвующих в презентации потенциально чужеродных антигенов, что необходимо для формирования адекватного иммунного ответа. При иммунофенотипировании может быть использован в качестве маркёра активированных клеток. CD3+HLA-DR+ — клетки, представляющие собой зрелые активированные Т-лимфоциты человека. CD3-HLA-DR+ — активированные клетки, не относящиеся к Т-лимфоцитам (В-лимфоциты и активированные ЕК).
Способность лимфоцитов к активации.
Способность лимфоцитов к активации в данном тесте оценивают по содержанию лимфоцитов, экспрессирующих CD69 в ответ на инкубацию в присутствии ФГА (митоген растительного происхождения). CD69 (другие названия — activation inducer molecule, AIM; early activation antigen, EA-1) – ранний маркёр активации, трансмембранный белок типа I. Этот белок вовлечен в ранние механизмы активации Т-клеток, ЕК-клеток, В-клеток, моноцитов и тромбоцитов.
Фагоцитарная активность лейкоцитов.
Данные по фагоцитарной активности нейтрофилов и моноцитов (относительное содержание клеток, фагоцитировавших добавленные к пробе при инкубации меченые флюоресцентной меткой бактерии) позволяют оценить резервные возможности этих клеток по поглощению и перевариванию чужеродных агентов.
Циркулирующие иммунные комплексы общие (ЦИК)
Одновременное присутствие высоких концентраций антигенов и их специфических антител может вести к образованию циркулирующих иммунных комплексов. Иммунные комплексы могут выходить из кровотока в мелких сосудах и откладываться в тканях, например, в гломерулах почек, в лёгких, коже, суставах, стенке сосудов. ЦИК обладают способностью связывать и активировать комплемент, что ведёт к повреждению ткани. Повышение уровня ЦИК может наблюдаться при аутоиммунных заболеваниях, хронических инфекционных заболеваниях, при которых постоянная продукция антигена инфекционным агентом сочетается с иммунным ответом на него (хронические гепатиты). Клинически это часто проявляется гломерулонефритами, артритами, нейропатиями. Несмотря на непосредственную роль в патогенезе некоторых заболеваний, определение ЦИК не всегда информативно, поскольку количество иммунных комплексов, отложившихся в тканях более важно, чем количество комплексов, циркулирующих в крови. Исследование ЦИК может быть недостаточно чувствительным и специфичным в диагностике болезней, вызываемых иммунными комплексами, и должно дополняться исследованием эффектов ЦИК на функцию органов (например, концентрация креатинина и анализ мочи), а также определением С3 С4 компонентов комплемента (см. тест
№ 193
), количество которых снижается вследствие усиленного потребления.
Данные иммунологического исследования интерпретирует врач-иммунолог в комплексе со всеми клинико-анамнестическими данными конкретного пациента. При оценке иммунного статуса пациента результаты исследования оценивают с точки зрения природы и стадии патологического процесса, сопутствующих заболеваний, приёма лекарственных препаратов и пр. При этом важны не только абсолютные значения отдельных показателей, но и их соотношение и динамика показателей. Изменения иммунологических показателей могут быть проявлением нормальной реакции организма на воздействие физиологических или патологических факторов (с различной картиной сдвигов на разных стадиях заболевания), отражать чрезмерную активацию, истощение иммунной системы, характеризовать врождённый или приобретённый дефект отдельных звеньев иммунной системы.
Литература
- Зурочка А.В., Хайдуков С.В. и др. — Проточная цитометрия в медицине и биологии. – Екатеринбург: РИО УрО РАН, 2013. – 552 с.
- Клиническая иммунология и аллергология / Ред. Лолор-младший Г., Фишер Т, Д. Адельман Д../: Пер. с англ. — М.: Практика, 2000. — 806 с.
- Клиническая лабораторная диагностика. Национальное руководство. Том 2./Ред. Долгов В.В., Меньшиков В.В./ – М., ГЭОТАР-Медиа, 2012 – 808 с.
- Практическое руководство по детским болезням. Том 8 Иммунология детского возраста. /Ред. А.Ю.Щербина, Е.Д.Пашанов/ — Москва: МЕДПРАКТИКА, 2006 — 432 с.
- Ройт А., Бростофф Д., Дейл Д. Иммунология. — М.: Мир, 2000 — 592 с
- Ярилин А. А. Иммунология. – М.: ГЭОТАР-Медиа. 2010 — 752 с.
- Leach М., Drummond М., Doig A. Practical Flow Cytometry in Haematology Diagnosis Hardcover. – WILEY-BLACKWELL, 2013.
- Tietz Clinical guide to laboratory tests. 4-th ed. Ed. Wu A.N.B. – USA: W.B Sounders Company, 2006 — 1798 p.
Источник
Метод определения
Субпопуляции лимфоцитов: иммунофенотипирование (проточная цитофлуориметрия, безотмывочная технология).
Фагоцитарная активность: оценка фагоцитоза бактерий с флуоресцентной меткой.
Циркулирующие иммунные комплексы (ЦИК): спектрофотометрия.
Иммуноглобулины A, M, G: иммунотурбидиметрия.
Иммуноглобулин E: хемилюминесцентный иммуноанализ.
Исследуемый материал
Цельная кровь с ЭДТА, цельная кровь с гепарином, сыворотка крови
Скрининговая оценка состояния различных звеньев иммунитета, используемая в диагностике первичных и вторичных иммунодефицитов, аутоиммунных, лимфопролиферативных, инфекционных, гематологических заболеваний.
В состав скринингового исследования входят следующие показатели:
- Лимфоциты , абсолютное значение
- Субпопуляции лимфоцитов:
- Т-лимфоциты (CD3+)
- Т-хелперы (CD3+CD4+)
- Т-цитотоксические лимфоциты (CD3+CD8+)
- Иммунорегуляторный индекс (CD3+CD4+/CD3+CD8+)
- В-лимфоциты (СD19+)
- ЕК-клетки (CD3-CD16+CD56+)
- Т-ЕК-клетки (CD3+CD16+CD56+)
- Фагоцитоз (гранулоциты)
- Фагоцитоз (моноциты)
- IgG
- IgA
- IgM
- IgE
Основные субпопуляции лимфоцитов:
Т-лимфоциты – лимфоциты, созревание которых происходит в тимусе (отсюда их название). Они контролируют работу В-лимфоцитов, ответственных за образование антител, т. е. за гуморальный иммунный ответ.
Т-хелперы, Th (от англ. to help – помогать) – разновидность Т-лимфоцитов, несут на своей поверхности структуры, способствующие распознаванию антигенов, презентированных вспомогательными клетками, участвуют в регуляции иммунного ответа, вырабатывая различные цитокины.
Цитотоксические Т-клетки — распознают фрагменты антигена, на поверхности клеток-мишеней, ориентируют свои гранулы по направлению к мишени и высвобождают их содержимое в области контакта с ней. При этом некоторые цитокины являются сигналом гибели (по типу апоптоза) для клеток-мишеней.
В-лимфоциты (от лат. «bursa» — сумка по названию сумки Фабрициуса, в которой созревают эти лимфоциты у птиц) проходят развитие в лимфоузлах и других периферических органах лимфоидной системы. На поверхности эти клетки несут иммуноглобулины, функционирующие как рецепторы к антигенам. В ответ на взаимодействие с антигеном В-лимфоциты отвечают делением и дифференциацией в плазматические клетки, вырабатывающие антитела, посредством которых обеспечивается гуморальный иммунитет.
ЕК-клетки (естественные клетки — киллеры) или натуральные киллеры-клетки с естественной, неиммунной цитотоксической активностью к неопластически изменённым клеткам-мишеням, которые не относятся ни к зрелым Т- или В-лимфоцитам, ни к моноцитам.
Т-ЕК-клетки (ЕКТ) – клетки с естественной неиммунной киллерной активностью, имеющие признаки Т-лимфоцитов.
Фагоцитарная активность лейкоцитов.
Данные по фагоцитарной активности нейтрофилов и моноцитов (относительное содержание клеток, фагоцитировавших добавленные к пробе при инкубации меченые флюоресцентной меткой бактерии) позволяют оценить резервные возможности этих клеток по поглощению и перевариванию чужеродных агентов.
Циркулирующие иммунные комплексы общие (ЦИК)
Одновременное присутствие высоких концентраций антигенов и их специфических антител может вести к образованию циркулирующих иммунных комплексов. Иммунные комплексы могут выходить из кровотока в мелких сосудах и откладываться в тканях, например, в гломерулах почек, в лёгких, коже, суставах, стенке сосудов. ЦИК обладают способностью связывать и активировать комплемент, что ведёт к повреждению ткани. Повышение уровня ЦИК может наблюдаться при аутоиммунных заболеваниях, хронических инфекционных заболеваниях, при которых постоянная продукция антигена инфекционным агентом сочетается с иммунным ответом на него (хронические гепатиты). Клинически это часто проявляется гломерулонефритами, артритами, нейропатиями. Несмотря на непосредственную роль в патогенезе некоторых заболеваний, определение ЦИК не всегда информативно, поскольку количество иммунных комплексов, отложившихся в тканях более важно, чем количество комплексов, циркулирующих в крови. Исследование ЦИК может быть недостаточно чувствительным и специфичным в диагностике болезней, вызываемых иммунными комплексами, и должно дополняться исследованием эффектов ЦИК на функцию органов (например, концентрация креатинина и анализ мочи), а также определением С3 С4 компонентов комплемента (см.
тест № 193
), количество которых снижается вследствие усиленного потребления.
Иммуноглобулины.
Данные иммунологического исследования интерпретирует врач-иммунолог в комплексе со всеми клинико-анамнестическими данными конкретного пациента. При оценке иммунного статуса пациента результаты исследования оценивают с точки зрения природы и стадии патологического процесса, сопутствующих заболеваний, приёма лекарственных препаратов и пр. При этом важны не только абсолютные значения отдельных показателей, но и их соотношение и динамика показателей. Изменения иммунологических показателей могут быть проявлением нормальной реакции организма на воздействие физиологических или патологических факторов (с различной картиной сдвигов на разных стадиях заболевания), отражать чрезмерную активацию, истощение иммунной системы, характеризовать врождённый или приобретённый дефект отдельных звеньев иммунной системы.
Литература
- Зурочка А.В., Хайдуков С.В. и др. — Проточная цитометрия в медицине и биологии. – Екатеринбург: РИО УрО РАН, 2013. – 552 с.
- Клиническая иммунология и аллергология / Ред. Лолор-младший Г., Фишер Т, Д. Адельман Д../: Пер. с англ. — М.: Практика, 2000. — 806 с.
- Клиническая лабораторная диагностика. Национальное руководство. Том 2./Ред. Долгов В.В., Меньшиков В.В./ – М., ГЭОТАР-Медиа, 2012 – 808 с.
- Практическое руководство по детским болезням. Том 8 Иммунология детского возраста. /Ред. А.Ю.Щербина, Е.Д.Пашанов/ — Москва: МЕДПРАКТИКА, 2006 — 432 с.
- Ройт А., Бростофф Д., Дейл Д. Иммунология. — М.: Мир, 2000 — 592 с
- Ярилин А. А. Иммунология. – М.: ГЭОТАР-Медиа. 2010 — 752 с.
- Leach М., Drummond М., Doig A. Practical Flow Cytometry in Haematology Diagnosis Hardcover. – WILEY-BLACKWELL, 2013.
- Tietz Clinical guide to laboratory tests. 4-th ed. Ed. Wu A.N.B. – USA: W.B Sounders Company, 2006 — 1798 p.
- Материалы фирм-производителей реагентов.
Источник
Метод определения
Гистологическое исследование биоптата согласно гистологической классификации Всемирной организации здравоохранения (ВОЗ) с окрашиванием гематоксилином-эозином.
ИГХ-исследование с применением спектра тканеспецифичных и прогностических антител (до пяти антител) (пероксидазный и авидин-биотиновый методы).
Исследуемый материал
Смотрите в описании
Комплексное исследование биоптатов метастатических образований различных локализаций, включающее морфологическое описание и оценку экспрессии спектра тканевых маркеров, для определения гистогенеза первичного опухолевого очага.
По статистике, в 3-15% случаев злокачественные опухоли манифестируют метастазами. Метастазы без выявленного первичного очага характеризуются случайной, нетипичной локализацией и быстрым прогрессированием процесса. Средняя продолжительность жизни пациентов с тремя и более метастатическими очагами поражения составляет три месяца. При этом локализация первичного очага у 60-70% пациентов выявляется только на аутопсии. Своевременная ИГХ-диагностика определяет тактику лечения до выявления первичного очага.
Патоморфологическая диагностика метастазов невыявленных опухолей предусматривает определение их морфологического типа, уточнение вероятного источника метастазирования, оценку злокачественного потенциала. Первая задача решается при рутинном гистологическом исследовании биопсийного материала (окрашивание гематоксилином-эозином), вторая – применением специальных методов исследования: гистохимического, иммуногистохимического (ИГХ) или молекулярно-генетического метода FISH (Fluorescence In Situ Hybridization).
При рутинной морфологической диагностике метастатические опухоли, согласно рекомендациям Европейского общества медицинской онкологии ESMO (European Society for Medical Oncology) (2004), разделяются на пять крупных категорий: аденокарцинома, плоскоклеточный рак, нейроэндокринный рак, недифференцированный рак, недифференцированная опухоль. Эти морфологические категории, наряду с данными о распространенности процесса, во многих случаях позволяют определить адекватный план обследования (и лечения). Так, например, при выявлении метастаза плоскоклеточного рака в шейных лимфатических узлах необходимо эндоскопическое обследования органов верхних дыхательных и пищеварительных путей. ИГХ-исследование, в зависимости от морфологического типа новообразования, позволяет уточнить гистогенез опухоли и/или определить вероятную локализацию первичного очага.
Для ИГХ-исследования первичных опухолей и их метастазов используется широкий спектр тканеспецифичных маркеров: -цитоспецифичные (кластеры дифференцировки лейкоцитов (CD – Clusters of Differentiation), гладкомышечный актин, миоглобин, тиреоглобулин); -маркеры пролиферации (Ki67, PCNA – Proliferating Cell Nuclear Antigen); -опухолевые маркеры – онкофетальные антигены (фетопротеин, карциноэмбриональный антиген); -гормоны (эстроген, прогестерон); -ферменты, белковые продукты клеточных онкогенов и др.
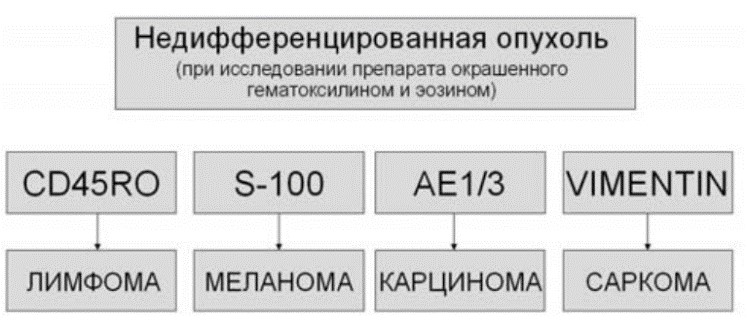
Единых алгоритмов при ИГХ-исследовании метастазов опухолей без уточненного первичного очага не разработано. Корректное определение направления дифференцировки опухолевых клеток и ряда биологических параметров опухоли само по себе является показанием для назначения определенных схем терапии. Например, обнаружение метастазов аденокарциномы в лимфоузлах подмышечной области может являться показанием к проведению терапии, аналогичной терапии рака молочной железы соответствующей стадии. Обнаружение экспрессии рецепторов эстрогенов и прогестерона в такой аденокарциноме может стать показанием к назначению антигормональной терапии вне зависимости от наличия определяемого опухолевого узла в молочной железе. Пример алгоритма, рекомендуемого для использования в дифференциальной диагностике.

Материал для исследования: биоптат опухоли, фиксированный в парафиновом блоке.
Литература
- Blaszyk H., Hartmann A., Bjornsson J. Cancer of unknown primary: clinicopathologic correlations. APMIS. 2003;111(12):1089-1094.
- Dabbs D.J. Diagnostic Immunohistochemistry: Theranostic and Genomic Applications. Elsevier, 4-th Edition. 2013:960.
- Di Patre P.L., Carter D. Sternberg’s Diagnostic Surgical Pathology Review. Wolters Kluver, 2-nd Edition. 2015:488.
- Dietal M., Wittekind С., Bussolati G., von Winterfeld М. Pre-Analytics of Pathological Specimens in Oncology. Sрringer. 2015:133.
- Dodd L.G, Bui M.М. Atlas of Soft Tissue and Bone Pathology. DemosMEDICAL. 2014:720.
- Edge S.B, Byrd D.R., Compton C.C., Fritz A.G., Greene F.L., Trotti A. AJCC Cancer Staging Manual. Sрringer, 7-th Edition. 2011:646.
- Elder D.E. Lever’s Histopathology of the Skin. Wolters Kluver, 11-th Edition. 2014:1544.
- Epstein J., Netto G. Biopsy Interpretation of the Prostate. Lippincott Williams and Wilkins, 5-th Edition. 2014:450.
- Erickson L. Atlas of Endocrine Pathology. Sрringer, 1-st Edition. 2014:178.
- ESMO Minimum Clinical Recommendations for diagnosis, treatment and follow-up of cancers of unknown primary site. Annals of Oncology. 2005;16(S.1):175-176.
- Fletcher C.D.M., Bridge J.A., Hogendoorn P., Mertens F. WHO Classification of Tumours of Soft Tissue and Bone. WHO Press, 4-th Edition. 2013;5:427.
- Kurman R.J., Carcangiu M.L., Herrington C.S., Young R.H. WHO Classification of Tumours of the Female Reproductive Organs. WHO Press, 4-th Edition. 2014;4:316.
- Louis D.N., Ohgaki H., Wiestler O.D., Cavenee W.K. WHO Classification of Tumours of the Central Nervous System. WHO Press, 4-th Edition. 2007;1:312.
- Malpica A., Euscher Е.D. Biopsy Interpretation of the Uterine Cervix and Corpus. Wolters Kluver, 2-nd Edition. 2015:368.
- Nishizuka S., Chen S.T., Gwadry F. et al. Diagnostic markers that distinguish colon and ovarian adenocarcinomas: identification by genomic, proteomic, and tissue array profiling. Cancer Research. 2003;63:5243-5250.
- Nordi Q.C. https://www.nordiqc.org.
Источник

