Гемосиндром анализ крови в инвитро
Метод определения
См. в описании
Исследуемый материал
Смотрите в описании
Кровь — это жидкая ткань, выполняющая различные функции, в том числе, транспорта кислорода и питательных веществ к органам и тканям и выведения из них шлаковых продуктов. Состоит из плазмы и форменных элементов: эритроцитов, лейкоцитов и тромбоцитов.

Общий анализ крови в лаборатории ИНВИТРО включает в себя определение концентрации гемоглобина, количества эритроцитов, лейкоцитов и тромбоцитов, величины гематокрита и эритроцитарных индексов (MCV, RDW, MCH, MCHC). Общий анализ — см. тест № 5, Лейкоцитарная формула — см. тест № 119, СОЭ — см. тест № 139.
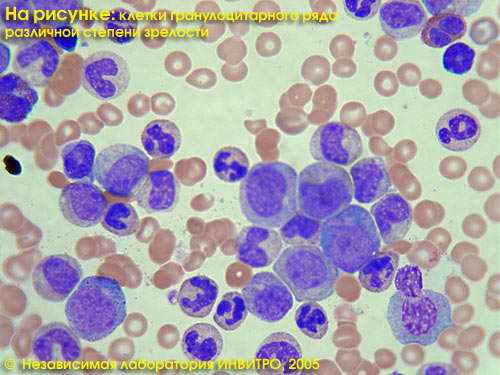
Лейкоцитарная формула — это процентное соотношение различных видов лейкоцитов (нейтрофилы, лимфоциты, эозинофилы, моноциты, базофилы).
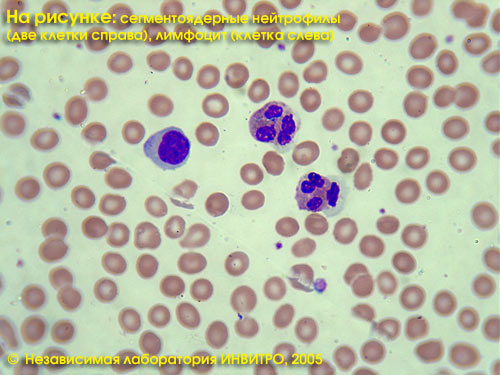
Лейкоцитарная формула в Независимой лаборатории ИНВИТРО включает в себя определение (в %) нейтрофилов, лимфоцитов, эозинофилов, базофилов, моноцитов. Общий анализ — см. тест № 5, Лейкоцитарная формула — см. тест № 119, СОЭ — см. тест № 139.
Скорость оседания эритроцитов (СОЭ) — неспецифический показатель воспаления. СОЭ — показатель скорости разделения крови в пробирке с добавленным антикоагулянтом на 2 слоя: верхний (прозрачная плазма) и нижний (осевшие эритроциты). Скорость оседания эритроцитов оценивается по высоте образовавшегося слоя плазмы (в мм) за 1 час. Удельная масса эритроцитов выше, чем удельная масса плазмы, поэтому в пробирке при наличии антикоагулянта (цитрата натрия) под действием силы тяжести эритроциты оседают на дно.
Процесс оседания (седиментации) эритроцитов можно разделить на 3 фазы, которые происходят с разной скоростью. Сначала эритроциты медленно оседают отдельными клетками. Затем они образуют агрегаты — «монетные столбики», и оседание происходит быстрее. В третьей фазе образуется очень много агрегатов эритроцитов, их оседание сначала замедляется, а потом постепенно прекращается.
Показатель СОЭ меняется в зависимости от множества физиологических и патологических факторов. Значения СОЭ у женщин несколько выше, чем у мужчин. Изменения белкового состава крови при беременности ведут к повышению СОЭ в этот период.
Снижение содержания эритроцитов (анемия) в крови приводит к ускорению СОЭ и, напротив, повышение содержания эритроцитов в крови замедляет скорость седиментации. В течение дня возможно колебание значений, максимальный уровень отмечается в дневное время. Основным фактором, влияющим на образование «монетных столбиков» при оседании эритроцитов является белковый состав плазмы крови. Острофазные белки, адсорбируясь на поверхности эритроцитов, снижают их заряд и отталкивание друг от друга, способствуют образованию «монетных столбиков» и ускоренному оседанию эритроцитов.
Повышение белков острой фазы, например, С-реактивного белка, гаптоглобина, альфа-1-антитрипсина, при остром воспалении приводит к повышению СОЭ. При острых воспалительных и инфекционных процессах изменение скорости оседания эритроцитов отмечается через 24 часа после повышения температуры и увеличения числа лейкоцитов. При хроническом воспалении повышение СОЭ обусловлено увеличением концентрации фибриногена и иммуноглобулинов.
Определение СОЭ в динамике, в комплексе с другими тестами, используют в контроле эффективности лечения воспалительных и инфекционных заболеваний. Общий анализ — см. тест № 5, Лейкоцитарная формула — см. тест № 119, СОЭ — см. тест № 139.
Биоматериал – 2 пробирки:
Цельная кровь с ЭДТА
Цельная кровь с цитратом
Обращаем внимание, что при выполнении клинического анализа крови (
№1515
) и подсчете лейкоцитарной формулы (
№119
), если в пробах выявлены значимые отклонения и результат требует проведения ручной микроскопии, ИНВИТРО дополнительно бесплатно проводит ручной подсчет лейкоцитарной формулы с подсчетом молодых форм нейтрофилов (в том числе точным подсчетом палочкоядерных нейтрофилов) и количественной оценкой всех патологических форм лейкоцитов (при их наличии).
Источник
Метод определения
См. в описании
Исследуемый материал
Смотрите в описании
Кровь — это жидкая ткань, выполняющая различные функции, в том числе, транспорта кислорода и питательных веществ к органам и тканям и выведения из них шлаковых продуктов. Состоит из плазмы и форменных элементов: эритроцитов, лейкоцитов и тромбоцитов.

Общий анализ крови в лаборатории ИНВИТРО включает в себя определение концентрации гемоглобина, количества эритроцитов, лейкоцитов и тромбоцитов, величины гематокрита и эритроцитарных индексов (MCV, RDW, MCH, MCHC). Общий анализ — см. тест № 5, Лейкоцитарная формула —
см. тест № 911
, СОЭ — см. тест № 139.
Лейкоцитарная формула — это процентное соотношение различных видов лейкоцитов (нейтрофилы, лимфоциты, эозинофилы, моноциты, базофилы).

Лейкоцитарная формула в Независимой лаборатории ИНВИТРО включает в себя определение (в %) нейтрофилов, лимфоцитов, эозинофилов, базофилов, моноцитов. Общий анализ — см. тест № 5, Лейкоцитарная формула —
см. тест № 911
, СОЭ — см. тест № 139.
Скорость оседания эритроцитов (СОЭ) — неспецифический показатель воспаления. СОЭ — показатель скорости разделения крови в пробирке с добавленным антикоагулянтом на 2 слоя: верхний (прозрачная плазма) и нижний (осевшие эритроциты). Скорость оседания эритроцитов оценивается по высоте образовавшегося слоя плазмы (в мм) за 1 час. Удельная масса эритроцитов выше, чем удельная масса плазмы, поэтому в пробирке при наличии антикоагулянта (цитрата натрия) под действием силы тяжести эритроциты оседают на дно.
Процесс оседания (седиментации) эритроцитов можно разделить на 3 фазы, которые происходят с разной скоростью. Сначала эритроциты медленно оседают отдельными клетками. Затем они образуют агрегаты — «монетные столбики», и оседание происходит быстрее. В третьей фазе образуется очень много агрегатов эритроцитов, их оседание сначала замедляется, а потом постепенно прекращается.
Показатель СОЭ меняется в зависимости от множества физиологических и патологических факторов. Значения СОЭ у женщин несколько выше, чем у мужчин. Изменения белкового состава крови при беременности ведут к повышению СОЭ в этот период.
Снижение содержания эритроцитов (анемия) в крови приводит к ускорению СОЭ и, напротив, повышение содержания эритроцитов в крови замедляет скорость седиментации. В течение дня возможно колебание значений, максимальный уровень отмечается в дневное время. Основным фактором, влияющим на образование «монетных столбиков» при оседании эритроцитов является белковый состав плазмы крови. Острофазные белки, адсорбируясь на поверхности эритроцитов, снижают их заряд и отталкивание друг от друга, способствуют образованию «монетных столбиков» и ускоренному оседанию эритроцитов.
Повышение белков острой фазы, например, С-реактивного белка, гаптоглобина, альфа-1-антитрипсина, при остром воспалении приводит к повышению СОЭ. При острых воспалительных и инфекционных процессах изменение скорости оседания эритроцитов отмечается через 24 часа после повышения температуры и увеличения числа лейкоцитов. При хроническом воспалении повышение СОЭ обусловлено увеличением концентрации фибриногена и иммуноглобулинов.
Определение СОЭ в динамике, в комплексе с другими тестами, используют в контроле эффективности лечения воспалительных и инфекционных заболеваний. Общий анализ — см. тест № 5, Лейкоцитарная формула —
см. тест № 911
, СОЭ — см. тест № 139.
Биоматериал – 2 пробирки:
Цельная кровь с ЭДТА
Цельная кровь с цитратом
Обращаем внимание, что при выполнении клинического анализа крови (
№1515
) и подсчете лейкоцитарной формулы (
№119
), если в пробах выявлены значимые отклонения и результат требует проведения ручной микроскопии, ИНВИТРО дополнительно бесплатно проводит ручной подсчет лейкоцитарной формулы с подсчетом молодых форм нейтрофилов (в том числе точным подсчетом палочкоядерных нейтрофилов) и количественной оценкой всех патологических форм лейкоцитов (при их наличии).
*просмотр мазка крови под микроскопом врачом-гематологом с дополнительным уточнением лейкоцитарной формулы и описанием морфологии клеток.
Источник
Метод определения
Real-time-PCR.
Исследуемый материал
Цельная кровь (с ЭДТА)
Расширенное исследование генов системы гемостаза: F2, F5, MTHFR, MTR, MTRR, F13, FGB, ITGA2, ITGВ3, F7, PAI-1
Комплексное исследование генетических факторов риска развития нарушений в системе свертывания крови и фолатном цикле.
Различные изменения в генах системы гемостаза и цикла обмена фолатов предрасполагают к развитию большого числа патологических состояний: инфаркты, инсульты, тромбоэмболии, кровотечения, патология беременности и родов, осложнения послеоперационного периода и т.д.
Профиль включает в себя исследование основных полиморфизмов в генах системы гемостаза и фолатного цикла:
- F2 c.*97G>A (20210 G>A; rs1799963),
- F5 c.1601G>A (Arg534Gln; 1691 G>A; rs6025),
- MTHFR c.665C>T (Ala222Val; 677 C>T; rs1801133),
- MTHFR c.1286A>C (Glu429Ala; 1298 A>C; rs1801131),
- MTR c.2756A>G (Asp919Gly; rs1805087),
- MTRR c.66A>G (Ile22Met; rs1801394),
- F13 с.103G>T (I63Т; rs5985),
- FGB c.-467G>A (-455 G>А; rs1800790),
- ITGA2 c.759C>T (Phe253Phe, 807 C>T; rs1126643),
- ITGB3 c.176T>C (Leu59Pro; 1565 T>C; rs5918),
- F7 c.1238G>A (Arg353Gln; 10976 G>A; rs6046),
- PAI-1 (SERPINE1) –675 5G>4G (rs1799889).
Ген F2 кодирует аминокислотную последовательность белка протромбина. Полиморфизм F2 c.*97G>A приводит к повышенной экспрессии гена. Клинически неблагоприятный вариант полиморфизма (c.*97A) наследуется по аутосомно-доминантному типу. Наличие полиморфизма F2 c.*97G>A в гомозиготной или гетерозиготной форме значительно (в 3 и более раз, а на фоне курения — в 40 и более раз) увеличивает риск возникновения венозных тромбозов, в том числе тромбозов сосудов мозга и сердца, особенно в молодом возрасте. У пациентов-носителей данного полиморфизма повышен риск развития тромбоэмболий после хирургических вмешательств. Приём оральных контрацептивов у данной группы лиц также увеличивает риск тромбозов (относительный риск развития тромбофилии и венозной тромбоэмболии у гетерозиготных носительниц полиморфизма c.*97G>A возрастает в 16 раз).
Ген F5 кодирует аминокислотную последовательность белка проакцелерина — коагуляционного фактора 5. Нуклеотидная замена c.1601G>A («мутация Лейден») приводит к аминокислотной замене аргинина на глутамин в позиции 534, что придает устойчивость активной форме проакцелерина. Клинически это проявляется рецидивирующими венозными тромбозами и тромбоэмболиями. Наличие полиморфизма в гомозиготной или гетерозиготной форме значительно (в 3 и более раз, а на фоне заместительной гормонотерапии или приема оральных контрацептивов — в 30 и более раз) увеличивает риск венозных тромбозов. Риск инфаркта миокарда увеличивается в 2 и более раз, риск развития патологии беременности (прерывание беременности, преэклампсия, хроническая плацентарная недостаточность и синдром задержки роста плода) увеличивается в 3 и более раз.
Также, пациенты, являющиеся одновременно носителями полиморфизма c.*97G>A гена протромбина и «мутации Лейден», еще в большей степени подвержены риску развития тромбозов и тромбоэмболий.
Ген MTHFR кодирует аминокислотную последовательность фермента метилентетрагидрофолатредуктазы, играющего ключевую роль в метаболизме фолиевой кислоты. Полиморфизм c.665C>T гена MTHFR связан с заменой нуклеотида цитозина (С) на тимин (Т), что приводит к аминокислотной замене аланина на валин в позиции 222. Вариант c.665Т связан с четырьмя группами мультифакториальных заболеваний: сердечно-сосудистыми, дефектами развития плода, колоректальной аденомой и раком молочной железы и яичников. У женщин с генотипом c.665Т/Т дефицит фолиевой кислоты во время беременности может приводить к порокам развития плода, в том числе незаращению нервной трубки. Неблагоприятное воздействие варианта c.665Т- зависит от внешних факторов: низкого содержания в пище фолатов, курения, приема алкоголя. Сочетание генотипа c.665Т/Т и папилломавирусной инфекции увеличивает риск цервикальной дисплазии. Назначение препаратов фолиевой кислоты может значительно снизить негативное влияние данного варианта полиморфизма.
Полиморфизм MTHFR c.1286A>C связан с точечной заменой нуклеотида аденина (А) на цитозин (С), что приводит к замене аминокислотного остатка глутаминовой кислоты на аланин в позиции 429, относящейся к регулирующей области молекулы фермента. При наличии данного полиморфизма отмечается снижение активности фермента MTHFR. Это снижение обычно не сопровождается изменением уровня гомоцистеина в плазме крови у носителей дикого варианта полиморфизма c.665C>T, однако сочетание аллельного варианта* c.1286C с аллелем c.665T приводит к снижению уровня фолиевой кислоты и соответствует по своему эффекту гомозиготному состоянию MTHFR c.665Т/T. При этом риск развития дефектов нервной трубки повышается в 2 раза. Жизнеспособность плодов, имеющих одновременно оба полиморфных варианта, также снижена.
Ген MTR кодирует аминокислотную последовательность фермента метионин синтазы. Полиморфизм c.2756A>G связан с аминокислотной заменой (аспарагиновой кислоты на глицин) в молекуле фермента. В результате этой замены функциональная активность фермента изменяется, что приводит к повышению риска формирования пороков развития у плода. Влияние полиморфизма усугубляется повышенным уровнем гомоцистеина.
Ген MTRR кодирует аминокислотную последовательность фермента редуктазы метионинсинтазы. Полиморфизм c.66A>G связан с аминокислотной заменой в молекуле фермента. В результате этой замены функциональная активность фермента снижается, что приводит к повышению риска развития дефектов нервной трубки у плода. Влияние полиморфизма усугубляется дефицитом витамина В12. При сочетании полиморфизма c.66A>G гена MTRR с полиморфизмом c.665C>T в гене MTHFR риск spina bifida увеличивается. Полиморфизм c.66A>G гена MTRR усиливает гипергомоцистеинемию, вызываемую полиморфизмом c.665C>T в гене MTHFR.
Ген фибриназы (F13) кодирует синтез трансглютаминазы, участвующей в стабилизации фибринового сгустка и в формировании соединительной ткани. Аллельные варианты с.103G/Т и с.103Т/Т приводят к снижению уровня трансглютаминазы с образованием сетчатой структуры фибрина с более тонкими волокнами, меньшими порами, и изменением характеристик проникновения, которое в сочетании с другими факторами риска ассоциируется с возможным риском внутричерепных кровоизлияний и кровотечений из внутренних органов, а также привычным невынашиванием беременности. При этом аллельный вариант с.103Т может выступать в роли протективного фактора в отношении инфаркта миокарда и венозных тромбозов.
Ген FGB кодирует β-цепь фибриногена, являющегося предшественником фибрина. Аллельный вариант c.-467А обусловливает усиленную транскрипцию гена и может приводить к увеличению уровня фибриногена в крови и повышению вероятности образования тромбов при наличии дополнительных факторов риска. Гетерозиготный вариант c.-467G/А связывают с повышенным риском ишемического инсульта и лакунарными инфарктами церебральных сосудов. Гомозиготный вариант c.-467A/А связывают с повышенным риском инфаркта миокарда.
Ген гликопротеина Gp1a (ITGA2) кодирует синтез альфа-2-субъединицы интегринов – специализированных рецепторов тромбоцитов. Аллельный вариант c.759Т вызывает изменение первичной структуры субъединицы и свойств рецепторов. При гетерозиготном (c.759C/T) варианте отмечается увеличение скорости адгезии тромбоцитов к коллагену I типа, что может приводить к повышенному риску тромбофилии, инфаркта миокарда и других сердечно-сосудистых заболеваний. Аллельный вариант c.759Т связывают со случаями резистентности к аспирину. Помимо этого, при гомозиготном (c.759Т/T) варианте значительно увеличивается количество рецепторов на поверхности тромбоцитов. В совокупности, при гомозиготном варианте данного полиморфизма значительно повышен риск тромбофилии, инфаркта миокарда и развития других острых эпизодов тромбообразования в возрасте до 50 лет, даже по сравнению с гетерозиготным вариантом.
Ген гликопротеина Gp3a (ITGB3) кодирует синтез бета-3 цепи интегринового комплекса GP2b3a, участвующего в разнообразных межклеточных взаимодействиях (адгезии и сигнализации).
Аллельный вариант c.176С (гетерозигота c.176T/C) обусловливает повышенную адгезию тромбоцитов и может приводить к увеличению риска развития острого коронарного синдрома, а также связан с синдромом привычного невынашивания беременности. Гомозиготный вариант c.176С/C обусловливает повышенную адгезию тромбоцитов и может приводить к значительному увеличению риска развития острого коронарного синдрома в возрасте до 50 лет. У лиц с полиморфными аллельными вариантами часто отмечается пониженная эффективность аспирина.
Аллельный вариант c.1238A (гетерозигота c.1238G/A и гомозигота c.1238А/A) гена F7 приводит к понижению экспрессии гена и снижению уровня фактора 7 в крови, рассматривается как протективный маркёр в отношении развития тромбозов и инфаркта миокарда.
Ген ингибитора активатора плазминогена (PAI-1) кодирует белок-антагонист тканевого и урокиназного активатора плазминогена. Преобладающим в популяции вариантом исследуемого полиморфизма является гетерозиготный вариант -675 5G/4G. В связи с этим данный полиморфизм самостоятельного диагностического значения не имеет, эффект возможно оценить в сочетании с другими факторами предрасполагающими к развитию патологии (например в сочетании с FGB c.-467A). Аллельный вариант -675 4G сопровождается большей активностью гена, чем -675 5G, что обусловливает более высокую концентрацию PAI-1 и уменьшение активности противосвёртывающей системы. Гомозигота -675 4G/4G ассоциирована с повышением риска тромбообразования, преэклампсии, нарушением функции плаценты и самопроизвольного прерывания беременности.
*Примечание: иногда в научной литературе при описании однонуклеотидных замен, характерных для генных полиморфизмов, встречается термин «мутантный аллель». Это терминологическая неточность, так как в классической генетике термин «мутантный аллель» традиционно рассматривается как синоним термина «мутация». При мутациях, как известно, изменение структуры гена приводит к образованию (экспрессии) нефункциональных белков и к неизбежному развитию наследственного заболевания. При полиморфизмах изменение в структуре гена приводит лишь к появлению белков с немного изменёнными физико-химическими свойствами. Такие изменения, как известно, проявляют себя при воздействии на организм различных факторов внешней среды или при изменении функционального состояния организма человека. И только в таких ситуациях функционирование белков со структурными особенностями может, либо способствовать ускорению развития заболевания, либо, напротив, тормозить формирование патологических процессов. Поэтому, на наш взгляд, для разграничения изменений в генах столь очень похожих структурно, но приводящих к несоизмеримо разным последствиям для организма, корректнее в отношении генных полиморфизмов применять понятие «аллельный вариант гена», а не «мутантный аллель».
Литература
- Никитина Л.А. и др. Роль некоторых генетических полиморфизмов в невынашивании беременности // Проблемы репродукции, 2007, С.83-89.
- Güngör et al. The presence of PAI-1 4G/5G and ACE DD genotypes increases the risk of early-stage AVF thrombosis in hemodialysis patients. // Ren Fail. 2011;33(2):169-7
- Wei YS, et al. Association of the integrin gene polymorphisms with ischemic stroke and plasma lipid levels // Zhonghua Yi Xue Yi Chuan Xue Za Zhi. 2009;26(2):211-5
- Gohil et al., The genetics of venous thromboembolism. A meta-analysis involving approximately 120,000 cases and 180,000 controls // Thromb Haemost, 2009. 102(2): 360-70
- Goodman et al., Which thrombophilic gene mutations are risk factors for recurrent pregnancy loss? // Am J Reprod Immunol, 2006. 56(4):230-6
- Gerhardt, A., et al. The polymorphism of platelet membrane integrin alpha2beta1 (alpha2807TT) is associated with premature onset of fetal loss // Thromb Haemost, 2005. 93(1):124-9.
- Ruzzi, L., et al., Association of PLA2 polymorphism of the ITGB3 gene with early fetal loss // Fertil Steril, 2005. 83(2): 511-2
- База OMIM: https://omim.org/entry/176930
- База OMIM: https://omim.org/entry/227400
- База OMIM +227400 https://omim.org/entry/607093
- База OMIM: https://omim.org/entry/602568
- База OMIM: https://omim.org/entry/156570
- https://www.ncbi.nlm.nih.gov/clinvar/RCV000012861/
Источник