Анализ крови на rh принадлежность
Крайне важное значение для клинической практики имеет определение антигенов эритроцитов – идентификация группы крови и резус-фактора. Группа крови человека определяется наличием на поверхности эритроцита антигенов и является индивидуальным признаком. Эритроцитарные поверхностные антигены эритроцитов определяет фенотип эритроцитов или группу крови человека.
В настоящее время известно более 200 антигенов эритроцитов, поэтому группа крови может отличаться в зависимости от количества используемых антисывороток для идентификации антигенов на поверхности эритроцитов. Эритроцитарные антигены, идентифицированные в популяции в 1% случаев, считаются редкими.
Основной системой идентификации групп крови является система АВО, в которой группа крови характеризуется наличием на поверхности эритроцитов антигенов А, В, АВ или их отсутствием (О), т.е. четыре группы крови. В некоторых руководствах встречается дополнительная маркировка групп крови: О (I); А(II); В (III) и АВ (IV).
Выявление в 1901 г. эритроцитарных антигенов положило начало изучению допустимости смешивания эритроцитов разных групп, т.е. совместимости гемотрансфузий. В крови (сыворотке) каждого индивидуума циркулируют антитела (называемые так же агглютинины), активные в отношении чужеродных антигенов. Взаимодействие антиген-антитело приводит к агглютинации (слипанию) и разрушению эритроцитов. В крови индивидуумов с группой крови А циркулируют антитела против антигенов В. Индивидуумы с группой крови В имеют антитела, против антигенов А. При группе крови О в сыворотке определяются антитела анти-А, анти-В, тогда как при группе крови АВ ни антитела А, ни антитела В в сыворотке не определяются.
Таким образом, индивидуумы с группой крови АВ являются универсальными реципиентами иногрупной крови.
Индивидуумы с группой крови О, эритроциты которых не имеют на поверхности ни А, ни В антигенов, являются универсальными донорами.
Антитела к эритроцитарным антигенам А или В являются генетически детерминированными, в соответствии с группой крови эритроцитов, тогда как антитела к другим поверхностным антигенам эритроцитов являются приобретенными. Пациенты, получающие трансфузии, со временем накапливают антитела, что может осложнять подбор требуемой группы крови. Для таких пациентов важно выполнять типирование группы крови с оценкой возможно большего спектра антител сыворотки.
Группа крови оценка совместимости
Для оценки совместимости групп крови и возможности трансфузий необходимо исследование реакции антител сыворотки донора и эритроцитов реципиента, а также эритроцитов донора и антител сыворотки реципиента.
При совместимости групп крови смешивание эритроцитов и сыворотки не приводит к изменению состава и окраски реакционной капли.
При несовместимости групп смешивание эритроцитов донора и сыворотки пациента вызывает реакцию агглютинации – образование в капле неоднородностей в виде слипшихся эритроцитов, точечно насыщающих поле реакции.
Резус-фактором (Rh) называют антиген D, который может располагаться на поверхности эритроцитов. Наличие или отсутствие этого антигена на поверхности эритроцитов индивидуума определяет такую характеристику группы крови, как резус положительная или резус отрицательная (Rh+ или Rh–). Примерно 85% популяции людей имеют резус-положительную группу крови (Rh+).
В отличие от антител к антигенам АВ, антитела к антигену D не присутствуют в крови. При контакте крови резус-положительной группы с резус-отрицательной, происходит сенсибилизация и синтез анти-резусных антител. Такая реакция развивается, например, при беременности Rh– матери Rh+ плодом. Выход фетальных клеток во время родов в кровоток матери активизирует синтез антирезусных антител. В случае пересечения антирезусными антителами плацентарного барьера и попадания в кровь плода, развивается гемолитическая желтуха новорожденного, обусловленная разрушением эритроцитов.
Определение резус фактора необходимо для каждого индивидуума в дополнение к определению группы крови. Отмечено, что выраженность структуры эритроцитарного антигена различна у здоровых людей и тем более у иммуноскомпроментированных больных, беременных женщин.
В настоящее время определение групп крови, резус фактора, продукции антиэритроцитарных антител выполняется в автоматическом режиме стандартизированными методами, позволяющими одномоментно проводить как типирование групп крови, определение продукции антител, так и совместимости возможных трансфузий. Визуальное отображение полученной карты для каждого пациента может быть востребовано в течение всей жизни пациента, она хранится в базе данных лаборатории.
Показания к исследованию: Любое стационарное лечение, беременность.
Условия взятия и хранения образца
Для исследования используется венозную кровь, взятую с ЭДТА или без консервантов. Взятие крови производится натощак, или не менее чем через 8 ч после последнего приема пищи. Образец крови может храниться при температуре от 4–8 °С не более 24 ч.
Результаты исследованияГруппа крови системы АВО:
- 0 (I) – первая группа;
- A (II) – вторая группа;
- B (III) – третья группа;
- AB (IV) – четвертая группа крови.
При выявлении подтипов (слабых вариантов) групповых антигенов результат выдается с соответствующим комментарием, например, «выявлен ослабленный вариант А2, необходим индивидуальный подбор компонентов крови».
Резус принадлежность
- Rh (+) положительная;
- Rh (–) отрицательная.
При выявлении слабых и вариантных подтипов антигена D выдается комментарий: «выявлен слабый резус-антиген, рекомендуется при необходимости выполнять трансфузию резус-отрицательных компонентов крови».
Источник
Метод определения
магнитизация эритроцитов, метод гель-фильтрации с использованием моноклональных антител. Автоматические анализаторы QWALYS (Diagast), IH-1000 (Bio-Rad).
Исследуемый материал
Цельная кровь (с ЭДТА)
Тест предназначен для определения резус-принадлежности потенциальных реципиентов (обследование перед госпитализацией) и беременных или планирующих беременность женщин.
Резус (Rh) – одна из важнейших систем эритроцитарных антигенов (наряду с системой АВ0), клинически значимая не только для безопасного переливания крови, но и при ведении беременности (при оценке возможности возникновения резус-конфликта и риска развития гемолитической болезни плода и новорожденного).
Антиген RhD является наиболее иммуногенным* из антигенов системы резус, его наличие на поверхности эритроцитов обуславливает положительную резус-принадлежность. Наличие этого структурного белка мембраны эритроцитов является генетически наследуемым признаком. В составе антигена RhD выделяют структурные единицы – эпитопы (в настоящий момент определены 36 структурных единиц).
Резус-отрицательные пациенты развивают иммунный ответ, сопровождаемый выработкой антирезусных антител, при переливании им резус-положительной крови. Наличие анти-резус антител ведет к разрушению эритроцитов, несущих резус-антиген, и к тяжелым пост-гемотрансфузионным реакциям при повторных переливаниях резус-положительной крови резус-отрицательным реципиентам.
Аналогичный иммунный ответ может развивать резус-отрицательная женщина при беременности резус-положительным плодом. Несмотря на то, что обычно при беременности кровь плода не смешивается с кровью матери, в некоторых ситуациях (не первая по счету беременность, патологические состояния, связанные с изменением проницаемости плаценты, сенсибилизация после предшествующего переливания резус-положительной крови) иммунная система матери вырабатывает антитела к антигенам эритроцитов плода. Антитела разрушают резус-положительные эритроциты, что приводит к различным клиническим проявлениям (ранней потере плода, хроническому невынашиванию беременности) и к гемолитической болезни плода и новорожденных**.
У беременных женщин, имеющих резус-положительную принадлежность, проблем совместимости по резус-фактору с ребенком не возникает.
*Иммуногенность ‒ потенциальная способность антигена вызывать иммунный ответ (образование антител) у лиц, не имеющих этого антигена.
**Гемолитическая болезнь плода и новорожденных ‒ патологическое состояние плода или новорожденного, сопровождаемое гемолитической желтухой, анемией, нарушением рефлексов. Обусловлено иммунологическим конфликтом между матерью и плодом из-за несовместимости по эритроцитарным антигенам и связано с разрушением эритроцитов плода под действием антиэритроцитарных антител, поступающих через плаценту из крови матери в кровь ребенка. В большинстве случаев гемолитическая болезнь новорожденных обусловлена конфликтом по D-антигену. Но следует учесть, что возникновение данной патологии может быть обусловлено реакциями по АВ0-антигенам, а также несовместимостью по другим антигенам системы резус (С, Е, с, d, e) или М-, N-, Kell-, Duffy-, Kidd-антигенам (см. тест №15RH Rh (C, E, c, e), Kell – фенотипирование).
Оценка резус-принадлежности при беременности или подготовке к беременности, а также контроль наличия аллоиммунных антиэритроцитарных антител, включая антитела к RhD-антигену (см. тест № 140 Аллоиммунные антитела), важны для правильного ведения беременности резус-отрицательных женщин. Риск развития гемолитической болезни плода и новорожденного при повторных беременностях можно предотвратить своевременным введением Rh-иммуноглобулина.
Наследование резус-фактора
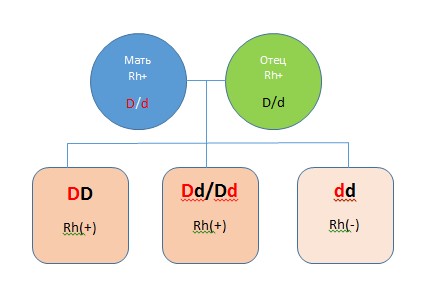
Генотип индивида состоит из двух гаплотипов, полученных по наследству: один от отца, другой от матери. Каждый гаплотип может обуславливать наличие антигенной детерминаты (D) или ее отсутствие (d). Доминантным является наличие антигенной детерминанты, следовательно:
| Генотип | Резус-принадлежность |
| DD | Rh-положительный |
| Dd | Rh-положительный |
| dd | Rh-отрицательный |
Таким образом, у родителей с положительной резус-принадлежностью могут рождаться дети с отрицательной резус-принадлежностью:

В случае когда резус-принадлежность будущего ребенка требует определения, необходимо использовать генеалогический или генетический метод (см. тест №7207 Определение генотипа резус-фактора).
Проблемы в определении резус-принадлежности
Большая часть резус-положительных лиц экспрессируют достаточное количество антигенных детерминант, содержащих все эпитопы. В этом случае при определении резус-принадлежности, вне зависимости от используемых тест-систем, проблем не возникает, и резус-принадлежность четко определяется как положительная. Однако у ряда лиц (не более 1% в европейской популяции) при определении резус-принадлежности могут возникать сложности по следующим причинам:
- Количество антигенных детерминант снижено в 3-10 раз, но структурно они не изменены. Такой вариант антигена называется слабым, D weak. Степень снижения количества детерминант разная, поэтому реакция агглютинации у таких пациентов может проходить с разной степенью выраженности.
- Количество антигенных детерминант может быть обычным, но они структурно изменены. На детерминантах антигена D отсутствуют некоторые эпитопы (одновременно может отсутствовать до 5 эпитопов). Такой вариант антигена называется неполным, вариантным или частичным, D partial. У человека выявлено более 10 таких форм антигена D. Наиболее часто встречаемым является вариант антигена DVI (встречаемость не более 0,1% в европейской популяции).
- Вариант резус-антигена D el характерен для азиатской популяции, встречаемость составляет до 30%. Проявляется очень низкой экспрессией антигена D на поверхности эритроцитов. Чаще всего обычными методами определяется как резус-отрицательный. С клинической точки зрения эти варианты важно отличать, особенно у женщин детородного возраста и при планировании переливания крови. При «неполном» варианте (D partial) возможно формирование антител к «полному» D антигену при переливании резус-положительной крови или гемокомпонентов. При «слабом» варианте (D weak) образование резус-антител маловероятно. Подход к выполнению исследования и к интерпретации результатов резус-принадлежности потенциальных реципиентов и потенциальных доноров отличается.
| Вариант антигена | Интерпретация для реципиента | Интерпретация для донора |
| D weak | Резус-принадлежность положительная, но при гемотрансфузии рекомендуется использовать резус-отрицательные эритроциты | Резус-принадлежность положительная |
| D partial (в том числе DVI) | Резус-принадлежность отрицательная | Резус-принадлежность положительная |
| D el | Резус-принадлежность отрицательная | Резус-принадлежность положительная |
Обратите внимание, что лаборатория ИНВИТРО исследует биоматериал только потенциальных реципиентов. Обследование потенциальных и действующих доноров требует применения принципиально других тест-систем и производится только на станциях переливания крови.
Литература
- Минеева П.В. Группы крови человека. Основы иммуногематологии. — СПб. 2004:188.
- Оловникова Н.И., Николаева Т.Л., Митерев Г. Ю. Иммуногематологическое обследование больных перед трансфузией донорских эритроцитов: пути оптимизации и улучшения качества тестирования. Справочник заведующего КДЛ. — М: Изд. МЦФЭР. 2014;6:33-46.
- Rizzo C. et al. Weak D and partial D: our experience in daily activity. Blood Transfusion. 2012;10:235-236.
- Westhoff С.М. The Structure and Function of the Rh antigen Complex. Seminars in Hematology. 2007;44(1):42-50.
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 27 марта 2019;
проверки требуют 57 правок.
Резус-фактор[1], или резус, Rh — одна из 36 систем групп крови, признаваемых Международным обществом трансфузиологов (ISBT). Клинически наиболее важная система после системы AB0.
Система резус-фактора состоит из групп крови, определяемых 59 антигенами, кодируемыми свыше 200 аллелями[2]. Наибольшее практическое значение для медицины имеют обладающие повышенными иммуногенными свойствами антигены: D, C, c, E, e. Часто используемые термины «резус-положительный» и «резус-отрицательный» относятся только, соответственно, к наличию или отсутствию антигена Rho(D), обладающего наибольшей иммуногенностью. Помимо своей роли в переливании крови, группы крови системы резус-фактора, в частности антиген Rho(D), является важной причиной гемолитической желтухи новорождённых или эритробластоза плода; для предотвращения этих заболеваний ключевым фактором является профилактика резус-конфликта. Риск резус-конфликта при беременности возникает у пар с резус-отрицательной матерью и резус-положительным отцом.
Группы крови системы резус-фактора встречаются у разных народностей и в разных регионах с разной частотой[3][4]. Резус-положительными являются около 85 % людей европеоидной расы[5][6].
Резус-фактор[править | править код]
В зависимости от человека, на поверхности эритроцитов может присутствовать или отсутствовать антиген Rho(D) системы резус-фактор, который является наиболее иммуногенным антигеном групп крови резус-системы. Как правило, статус обозначают суффиксом Rh+ для резус-положительной группы крови (имеется антиген Rho(D)) или резус-отрицательную группу крови (Rh-, нет антигена Rho(D)) после обозначения группы крови по системе AB0. Тем не менее, другие антигены этой системы группы крови также являются клинически значимыми. В отличие от системы групп крови AB0, активизация иммунного ответа против антигена системы резус-фактора в общем случае может иметь место только при переливании крови или плацентарном воздействии во время беременности.
Rh+ или Rh- в большинстве случаев, в том числе у реципиентов определяется по антигену Rho(D), вследствие его наибольшей антигенности из всех антигенов системы резус-фактора. Одновременно он может быть выражен в разной степени, в зависимости от экспрессии гена, его кодирующего. При стандартном методе определения антигена иногда может быть и ложноотрицательный результат, вызванный латентным проявлением гена (в случае Du, парциального эпитопа, Del, Rhnull). Сам антиген Rho(D) состоит из разных субъединиц RhA, RhB, RhC, RhD, отличающихся между собой, что, в свою очередь, может вызвать иммунный конфликт даже при попадании Rh+ крови с антигенном Rho(D), в структуре которого один тип субъединиц, в Rh+ организм с антигеном Rho(D), в структуре которого другой тип субъединиц. При определении резус-фактора доноров, кроме антигена Rho(D), определяют ещё наличие антигенов rh'(C) и rh»(E), Rh- донором считаются только те, у кого отсутствуют и эти антигены, так как они хоть в менее выраженной степени, но тоже способны вызывать иммунологическую реакцию при попадании в организм, в котором эти антигены отсутствуют. При наличии в организме женщины антигена Rho(D) любой степени выраженности она считается Rh+.
В отличие от системы группы крови AB0, в системе резус-фактора генами кодируются только антигены, при этом антиген представляет собой мембранный липопротеин. Антитела же появляются как иммунный ответ организма при введении крови, содержащей антиген, в организм человека, не содержащей этот антиген, в том числе при трансплацентарном попадании антигена, и относятся к IgM (при первичном резус-конфликте) и IgG (при повторных случаях).
Антиген rh'(С) встречается примерно у 70 % европеоидов, антиген hr'(c) — примерно у 80 %, rh»(E) — примерно у 30 %, антиген hr»(e) — примерно у 97 %. При этом их комбинации выявляются со следующей частотой: DCE — 15,85 % , DCe — 53,2 %, DcE — 14,58 %, Dce — 12,36 %. По данным исследований 1976 года у русских встречались следующие антигены с частотой: Rho(D) — 85,03 %, rh'(C) — 70,75 %, rh»(E) — 31,03 %, hr'(c) — 84,04 %, hr»(e) — 96,76 %[1].
История открытий[править | править код]
В 1939 году доктора Филип Левин и Руфус Стетсон опубликовали в первом докладе клинические последствия непризнаваемого резус-фактора в виде гемолитической реакции на переливание крови и гемолитической желтухи новорождённых в её наиболее тяжёлой форме[7]. Было признано, что сыворотка крови описываемой в докладе женщины вступила в реакцию агглютинации с красными кровяными тельцами примерно 80 % людей известных тогда групп крови, в частности, совпадающими по системе AB0. Тогда этому не было дано никакого названия, а позже такое стали называть агглютинин. В 1940 году доктора Карл Ландштейнер и Александр Винер опубликовали доклад о сыворотке, которая также взаимодействует примерно с 85 % различных эритроцитов человека[8]. Эта сыворотка была получена путём иммунизации кроликов с эритроцитами макаки-резуса. Антиген, вызвавший иммунизацию, назвали резус-фактором «для указания на то, что при изготовлении сыворотки был использован кровь макаки резус»[9].
Основываясь на серологическом сходстве, впоследствии резус-фактор также использовался для определения антигенов и анти-резуса для антител, обнаруживаемых у людей, подобно тому, как это ранее описано Левиным и Стетсоном. Хотя различия между двумя этими сыворотками были показаны уже в 1942 году и наглядно продемонстрированы в 1963 году, уже широко используемый термин «резус» сохранялся для клинического описания антител людей, которые отличаются от тех, что связаны с обезьянами-резусами. Этот действенный фактор, обнаруженный у макаки-резуса, был классифицирован системой антигена Ландштейнера-Винера (антиген LW, антитело анти-LW), названного в честь первооткрывателей[10][11].
Было признано, что резус-фактор был лишь одним в системе различных антигенов. Две различные терминологии были разработаны на основе разных моделей генетического наследования и обе все ещё используются.
Вскоре было понято клиническое значение этого антигена D с высокой степенью иммунизации. Была признана важность некоторых ключевых факторов при переливании крови, в том числе наличие надёжных диагностических тестов, а также требование учитывать вероятность появления гемолитической желтухи новорождённых, последствия переливания крови и необходимость предотвращения этого путём диспансеризации и профилактики.
Номенклатура Rh[править | править код]
Историческое обоснование фенотипов резус-фактора[править | править код]
Система резус-фактора групп крови имеет две номенклатуры: одна разработана Роналдом Фишером и Робертом Рэйсом[en] и другая Александром Винером[en]. Обе системы отражают альтернативные теории наследования. Система Фишера-Рэйса, чаще всего используемая сегодня, использует номенклатуру CDE. Эта система была основана на теории, что отдельный ген контролирует продукт каждого из соответствующих ему антигенов (например, ген D производит антиген D и так далее). Тем не менее, ген d был гипотетическим, а не реально существующим.
Система Винера использует номенклатуру Rh-Hr. Эта система основывается на теории, что было по одному гену в одиночном локусе на каждой хромосоме, каждая из которых производит несколько антигенов. По этой теории ген R1 предполагается привести к «факторам крови» Rh0, rh’ и hr’ (соответствующие современной номенклатуре антигенов D, C и E) и ген r, производящий hr’ и hr» (соответствующие современной номенклатуре из антигенов с и e)[12].
| по Фишеру-Рейсу | Dce | DCe | DcE | DCE | dce | dCe | dcE | dCE |
| по Винеру | Rh0 | R1 | R2 | RZ | r | r′ | r″ | rY |
Обозначение из двух теорий являются взаимозаменяемыми в пунктах сдачи крови (например, Rho(D) означает, что RhD положительно). Обозначения Винера более сложны и громоздки для повседневного использования. Поэтому теория Фишера-Рэйса, более просто объясняющая механизм, стала шире использоваться.
| Резус-принадлежность по антигену Rho(D) | Фенотип антигенов | Генотип хромосом | |
|---|---|---|---|
| по Фишеру-Рейсу | по Винеру | ||
| Rh+ | D, C, E, c, e | Dce/DCE | R0RZ |
| Dce/dCE | R0rY | ||
| DCe/DcE | R1R2 | ||
| DCe/dcE | R1r″ | ||
| DcE/dCe | R2r′ | ||
| DCE/dce | RZr | ||
| D, C, E, c | DcE/DCE | R2RZ | |
| DcE/dCE | R2rY | ||
| DCE/dcE | RZr″ | ||
| D, C, E, e | DCe/dCE | R1rY | |
| DCE/dCe | RZr′ | ||
| DCe/DCE | R1RZ | ||
| D, C, E | DCE/DCE | RZRZ | |
| DCE/dCE | RZrY | ||
| D, C, c, e | Dce/dCe | R0r′ | |
| DCe/dce | R1r | ||
| DCe/Dce | R1R0 | ||
| D, C, e | DCe/DCe | R1R1 | |
| DCe/dCe | R1r′ | ||
| D, E, c, e | DcE/Dce | R2R0 | |
| Dce/dcE | R0r″ | ||
| DcE/dce | R2r | ||
| D, E, c | DcE/DcE | R2R2 | |
| DcE/dcE | R2r″ | ||
| D, c, e | Dce/Dce | R0R0 | |
| Dce/dce | R0r | ||
| Rh- | C, E, c, e | dce/dCE | rrY |
| dCe/dcE | r′r″ | ||
| C, E, c | dcE/dCE | r″rY | |
| C, E, e | dCe/dCE | r′rY | |
| C, E | dCE/dCE | rYrY | |
| C, c, e | dce/dCe | rr′ | |
| C, e | dCe/dCe | r′r′ | |
| E, c, e | dce/dcE | rr″ | |
| E, c | dcE/dcE | r″r″ | |
| c, e | dce/dce | rr | |
Современные данные по геному резус-фактора[править | править код]
С развитием молекулярной генетики и расшифровкой генома человека в конце XX — начале XXI века стало известно[13], что структура антигена D кодируется геном RHD (англ.)русск.. При отсутствии или повреждении гена антиген не образуется, а при наличии гена антиген может как образовываться в разной степени выраженности, так и не образовываться. Образование антигена и его свойства зависят, в свою очередь, от гена RHAG, продуцирующего Rh-ассоциированный гликопротеин, который регулирует экспрессию гена RHD и RHCE. Ген RHCE (англ.)русск. кодирует структуру антигенов С, Е, с, е. Гены RHD и RHAG имеют большое сходство между собой по нуклеотидной последовательности и расположены в соседних локусах, частично перекрываясь. С генами и антигенами резус-фактора также ассоциированы CD47, гликофорин В, системы групп крови LW и Fy[2]. Ранее употреблявшееся обозначение антигена Du с 1992 года обозначается как Dweak (частичный антиген) и выделяют около 80 его вариантов[14][15].
Rhnull[править | править код]
Существуют задокументированные случаи отсутствия у людей Rh-антигенов. Всего в мире насчитывается около 50-ти человек с Rhnull — «отсутствующим» резус-фактором (из-за отсутствия Rh-антигенов (Rh или RhAG) в их кровяных клетках). Вследствие этого в данных кровяных клетках отсутствуют антигены LW и Fy5, а также слабо проявляются антигены S, s, и U[16]. Такая кровь может в редких случаях передаться по наследству, однако, как правило, является результатом двух совершенно случайных мутаций[17]. Около 9-ти человек в мире являются донорами крови с данным резус-фактором.
См. также[править | править код]
- Ген RHBG (англ.)русск.
- Ген RHCG (англ.)русск.
- Иммуноглобулин человека антирезус Rho(D) (англ.)русск.[18][19][20]
Примечания[править | править код]
- ↑ 1 2 Зотиков E. А. Резус-фактор // Большая медицинская энциклопедия, 3-е изд. — М.: Советская энциклопедия. — Т. 22.
- ↑ 1 2 Головкина Л. Л., Стремоухова А. Г., Пушкина Т. Д., Хасигова Б. Б., Атрощенко Г. В., Васильева М. Н., Каландаров Р. С., Паровичникова Е. Н. Молекулярные основы D-отрицательного фенотипа (обзор литературы и описание случаев) / Научная статья. ФГБУ «Гематологический научный центр» Минздрава России. // Журнал «Онкогематология», № 3. — 2015. Т. 10. С. 64—69. DOI: 10.17650/1818-8346-2015-10-3-64-69.
- ↑ Rh blood group system // Encyclopædia Britannica
- ↑ Давыдова Л. Е. Трансфузионно опасные антигены эритроцитов у якутов (частота и особенности распределения) / Диссертация по специальности 14.01.21 // ФГБУ «Гематологический научный центр» Минздрава России. 2015. — 137 с. (С. 7, 24—25, 27—35, 52, 63—68, 82, 85).
- ↑ Система резус (Rh) и другие
- ↑ Rh Blood Group System — Clinical Microbiology Syllabus
- ↑ Levine P., Stetson R. E. An unusual case of intragroup agglutination (англ.) // JAMA. — 1939. — Vol. 113. — P. 126—127.
- ↑ Landsteiner K., Wiener A. S. An agglutinable factor in human blood recognized by immune sera for rhesus blood (англ.) // Proc Soc Exp Biol Med (англ.)русск. : journal. — 1940. — Vol. 43. — P. 223—224.
- ↑ Landsteiner K., Wiener A. S. Studies on an agglutinogen (Rh) in human blood reacting with anti-rhesus sera and with human isoantibodies (англ.) // Journal of Experimental Medicine (англ.)русск. : journal. — Rockefeller University Press (англ.)русск., 1941. — Vol. 74, no. 4. — P. 309—320. — doi:10.1084/jem.74.4.309. — PMID 19871137.
- ↑ Avent N. D., Reid M. E. The Rh blood group system: a review (англ.) // Blood (англ.)русск.. — American Society of Hematology (англ.)русск., 2000. — Vol. 95, no. 2. — P. 375—387. — PMID 10627438.
- ↑ Scott M. L. The complexities of the Rh system (англ.) // Vox sang (англ.)русск. : journal. — 2004. — Vol. 87, no. (Suppl. 1). — P. S58—S62. — doi:10.1111/j.1741-6892.2004.00431.x.
- ↑ Weiner, Alexander S. (англ.)русск.. Genetics and Nomenclature of the Rh-Hr Blood Types (неопр.) // Antonie van Leeuwenhoek. — Netherlands: Springerlink, 1949. — 1 February (т. 15, № 1). — С. 17—28. — ISSN 0003-6072. — doi:10.1007/BF02062626.
- ↑ Тарлыков П. В., Кожамкулов У. А., Раманкулов Е. М. Генетические основы формирования групп крови человека / РГП «Национальный центр биотехнологии» // Журнал Биотехнология: теория и практика. 2014, № 2. — С. 4—10. УДК: 612:13: 616.1-078.
- ↑ Головкина Л. Л., Стремоухова А. Г., Пушкина Т. Д., Паровичникова Е. Н. Случай выявления антигена weak D type 4.2 (категория DAR) системы Резус / Научная статья. ФГБУ «Гематологический научный центр» Минздрава России. // Журнал «Онкогематология», № 3. — 2015. Т. 10. С. 70—72. DOI: 10.17650/1818-8346-2015-10-3-70-72.
- ↑ Шауцукова Л. З., Шогенов З. С. Система группы крови Rh (Резус): аналитический обзор // Журнал «Современные проблемы науки и образования». — 2015. — № 2 (часть 1). УДК 612.1. ISSN 2070-7428.
- ↑ Cartron, J.P. RH blood group system and molecular basis of Rh-deficiency (англ.) // Best Practice & Research Clinical Haematology. — 1999. — Декабрь (vol. 12, no. 4). — P. 655—689. — doi:10.1053/beha.1999.0047. — PMID 10895258.
- ↑ Самая драгоценная кровь на свете. Bird In Flight (8 сентября 2017). Дата обращения 6 сентября 2019.
- ↑ [1].
- ↑ [2].
- ↑ [3].
Литература[править | править код]
- Зотиков E. А. Резус-фактор // Большая медицинская энциклопедия, 3-е изд. — М.: Советская энциклопедия. — Т. 22.
- Головкина Л. Л. Резус-фактор // Большая российская энциклопедия : [в 35 т.] / гл. ред. Ю. С. Осипов. — М. : Большая российская энциклопедия, 2004—2017.
Ссылки[править | править код]
- О резус-факторе в BGMUT — медицинской базе данных о мутации антигена группы крови в НЦБИ, NIH (англ.) (Проверено 19 июля 2011)
- Статья в Нью-Йорк Таймс о первом упоминании резус-фактора (англ.) (Проверено 19 июля 2011)
Источник

