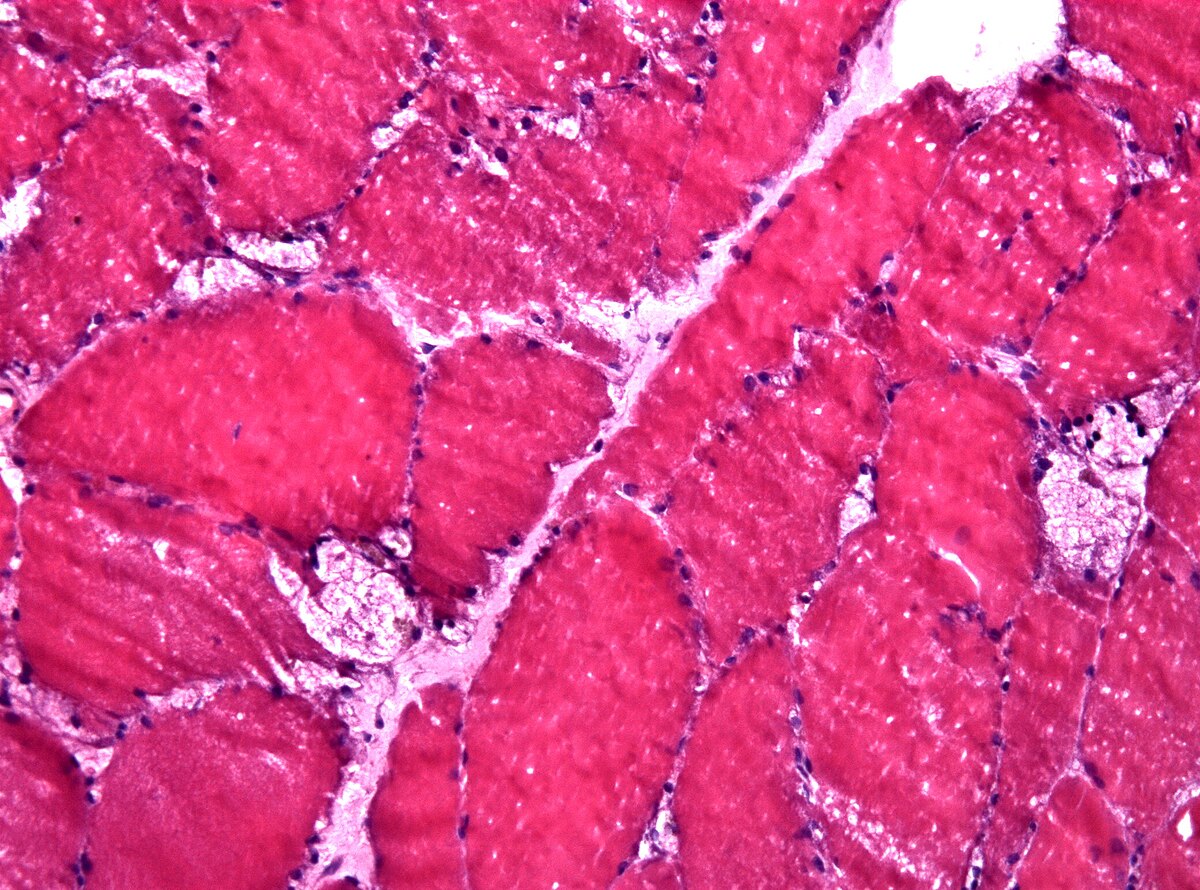
Анализ крови на активность кислой мальтазы
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 1 июня 2018;
проверки требуют 4 правки.
Боле́знь По́мпе (генерализо́ванный гликогено́з, гликогеноз II типа) — редкое наследственное заболевание с аутосомно-рецессивным механизмом наследования[1], связанное с повреждением мышечных и нервных клеток по всему организму. Клиническая картина данной патологии обусловлена накоплением гликогена в лизосомах, вызванным недостаточностью лизосомного фермента — кислой α-1,4-глюкозидазы. Различают быстро прогрессирующую (классическую) и медленно прогрессирующую формы болезни Помпе. Несмотря на широкий спектр клинических проявлений гликогеноза II типа, в основе всех форм болезни лежит дефицит одного фермента, кодируемого геном GAA.
Историческая справка[править | править код]
Данное заболевание было впервые описано в 1932 году голландским патологом И. К. Помпе[2][3]. В 1963 году бельгийский биохимик Генри Хэрс обнаружил у пациентов с этой болезнью недостаточность лизосомного фермента α-глюкозидазы[4]. Болезнь Помпе является первым наследственным заболеванием, идентифицированым как лизосомная болезнь накопления, которых сейчас описано около 50[5].
Эпидемиология[править | править код]
Распространённость болезни Помпе (гликогеноза II-го типа, англ. GSD II) составляет примерно 1 случай на 140 000 (классическая инфантильная форма) и 1 на 60 000 взрослого населения (болезнь Помпе с поздним началом)[6]. Заболевание встречается практически во всех этнических группах населения.
Наследование[править | править код]
Аутосомно-рецессивный механизм наследования болезни Помпе: оба родителя являются носителями дефектного гена (помечен красным кружочком). По законам Менделя вероятность рождения больного ребёнка составляет 25 %.
Заболевание наследуется по аутосомно-рецессивному типу и, таким образом, с одинаковой частотой встречается как у мужчин, так и у женщин.
Ген GAA, мутации в котором вызывают данное заболевание, локализован на аутосоме (хромосоме 17). Заболевание клинически манифестирует только в случае, когда обе аутосомы, полученные по одной от отца и матери, являются дефектными по данному гену. Как и во всех случаях аутосомно-рецессивного наследования, если оба родителя несут дефектный ген, то вероятность наследования болезни у потомства составляет 1 из 4. На схеме синим цветом обозначены здоровые, фиолетовым — носители дефектного гена, красным — болезнь Помпе (два дефектных гена одной аллели 17q25.2-3). Синим кружочком помечен нормальный ген, красным — дефектный.
Патогенез[править | править код]
Генетический дефект локуса 17q25.2-3 хромосомы (ген GAA) ведёт к дефициту кислой α-1,4-глюкозидазы (мальтазы) — одного из ферментов лизосом. В свою очередь дефект этого фермента вызывает прогрессирующее накопление гликогена, которое со временем может стать причиной необратимого поражения мышц и стать причиной смертельного исхода.
Диагностика[править | править код]
Диагноз данной редкой наследственной патологии верифицируется на основании лабораторного исследования степени активности фермента — кислой α-1,4-глюкозидазы (мальтазы) в крови (метод «сухого пятна»)[7] или тканях организма (кожных фибробластах, мышечной ткани, лейкоцитах).
Заболевание в встречается в различных клинических формах:
- классическая (инфантильная) форма болезни Помпе и
- болезнь Помпе с поздним началом (в детском, подростковом возрасте и у взрослых).
Этапы диагностического поиска[править | править код]
Классическая (инфантильная) форма:
- этап: выявление группы риска.
- основные клинические проявления:
- выраженная мышечная гипотония (синдром «вялого ребёнка»);
- задержка моторного развития;
- частые инфекционные заболевания верхних дыхательных путей (ОРЗ);
- наличие признаков дыхательной недостаточности;
- расстройства дыхания во сне;
- кардиомегалия в сочетании с кардиомиопатией;
- сердечная недостаточность;
- макроглоссия;
- гепатомегалия;
- спленомегалия;
- гипотрофия
- лабораторная диагностика: повышение уровня креатинфосфокиназы, лактатдегидрогеназы, АлАТ, АсАТ в сыворотке крови.
- инструментальные методы диагностики:
- поиск наличия признаков поражения миокарда и/или сердечного ритма;
- ЭКГ;
- ЭхоКГ;
- МРТ;
- рентгенография органов грудной полости
- основные клинические проявления:
- этап: специфическая диагностика.
- диагностика: для всех пациентов группы риска болезни Помпе — биохимический анализ активности кислой мальтазы в крови методом сухих пятен
- верификация: повторное измерение уровня активности кислой мальтазы в крови альтернативным методом (например, определение активности этого фермента в лейкоцитах периферической крови)
- этап: дополнительные методы диагностики.
- при наличии типичной клинической картины на фоне «нормальной» активности кислой мальтазы в крови показано проведение ДНК-диагностики дефектного гена (GAA).
- морфологический анализ мышечной ткани (биопсия) позволяет выявить специфические изменения, однако их отсутствие не исключает наличия болезни Помпе.
Диагностический алгоритм болезни Помпе с поздним началом:
- этап: выявление группы риска.
- основные клинические проявления:
- прогрессирующая мышечная слабость тазового и плечевого пояса (на начальных стадиях болезни преобладает слабость в ногах);
- затруднение при ходьбе, подъёме по лестнице, вставании из положения сидя;
- боли в мышцах;
- дыхательная недостаточность;
- ортопноэ;
- частые инфекционные заболевания дыхательных путей;
- дневная сонливость;
- головная боль по утрам;
- ночная гиповентиляция лёгких;
- снижение массы тела у детей и подростков;
- гипотрофия
- лабораторная диагностика: повышение уровня креатинфосфокиназы, лактатдегидрогеназы, АлАТ, АсАТ в сыворотке крови.
- инструментальные методы диагностики:
- выявление миопатического паттерна в ходе проведения миографии скелетных мышц конечностей;
- выявление расстройств дыхания во время сна (эпизоды апноэ и снижение степени оксигенации крови) в ходе проведения полисомнографии;
- выявление значительной разницы результатов измерения форсированной жизненной ёмкости лёгких (ФЖЕЛ) в положении лежа и сидя более, чем на 10 % от исходной величины ФЖЕЛ — ранний признак специфического поражения диафрагмы при болезни Помпе.
- основные клинические проявления:
- этап: специфическая диагностика.
- диагностика: для всех пациентов группы риска болезни Помпе — биохимический анализ активности кислой мальтазы в крови методом сухих пятен
- верификация: повторное измерение уровня активности кислой мальтазы в крови альтернативным методом (например, определение активности этого фермента в лейкоцитах периферической крови)
- этап: дополнительные методы диагностики.
- при наличии типичной клинической картины на фоне «нормальной» активности кислой мальтазы в крови показано проведение ДНК-диагностики дефектного гена (GAA).
- морфологический анализ мышечной ткани (биопсия) позволяет выявить специфические изменения, однако их отсутствие не исключает наличия болезни Помпе.
Клиническая картина[править | править код]
Накопление гликогена ведёт к развитию прогрессирующей мышечной слабости (миопатии). В патологический процесс вовлекаются различные органы и ткани макроорганизма: сердце, скелетные мышцы, печень и нервная система.
Встречаются исключения, однако уровень активности кислой α-1,4-глюкозидазы определяет форму гликогеноза II типа (англ. GSD II). В зависимости от возраста, в котором начинают проявляться клинические симптомы, выделяют две формы заболевания: классическую (или инфантильную) и болезнь Помпе с поздним началом — симптомы появляются позже и прогрессируют медленнее[8].
Классическая (инфантильная) форма[править | править код]
Начало клинических проявлений классической формы болезни, как правило, диагностируется в возрасте 4—8 месяцев. Обращает внимание задержка моторного развития ребёнка грудного возраста. При этом внешне мышцы ребёнка выглядят нормально, однако они вялые и слабые: ребёнок плохо держит голову, практически не переворачивается со спины на живот и обратно. По мере прогрессирования заболевания утолщается сердечная мышца и снижается её сократительная способность. Без лечения смерть обычно наступает в результате сердечной недостаточности и слабости дыхательных мышц[8].
Болезнь Помпе с поздним началом[править | править код]
Развитие клинической картины формы гликогеноза II-го типа с поздним началом происходит позже (в возрасте 1—2 лет), прогрессирует медленнее классической (инфантильной) формы. Одним из первых симптомов является прогрессирующее снижение силы мышц. Оно начинается с ног и распространяется на мышцы туловища и рук, в том числе диафрагму и другие мышцы, участвующие в акте дыхания. Наиболее распространённой причиной смерти является дыхательная недостаточность. В некоторых случаях отмечается увеличение размеров сердечной мышцы и наблюдаются нарушения сердечного ритма, однако это не относится к постоянным признакам данного заболевания[8].
Дифференциальная диагностика[править | править код]
К сожалению, диагноз устанавливается с задержкой, поскольку признаки и симптомы заболевания весьма похожи на проявления других болезней. Тем не менее, ранняя диагностика и специфическое лечение крайне необходимы для улучшения состояния пациента.
Дифференциальная диагностика гликогеноза II-го типа проводится:
- с другими лизосомными болезнями накопления: синдром Данона;
- с другими гликогенозами;
- с другими заболеваниями: полиомиозит, мышечная дистрофия Беккера — Дюшена, идиопатическая гипертрофическая кардиомиопатия, конечностно-поясная мышечная дистрофия.
Лечение[править | править код]
Существующие на сегодняшний день лечебные стратегии могут улучшить качество жизни пациентов с гликогенозом II-го типа, однако они не способны изменить течение болезни. Раннее начало терапии чрезвычайно важно для достижения наибольшего эффекта.
Единственный вариант специфического лечения заболевания — терапевтическое замещение повреждённого либо отсутствующего фермента фармацевтическим препаратом «Майозайм» (альглюкозидаза альфа, rhGAA). Данный препарат разработан компанией «Genzyme Corp.» и успешно прошёл клинические испытания, в которых участвовало 39 больных в возрасте от 1 месяца до 3.5 лет. В 2006 году он был одобрен FDA для лечения пациентов с инфантильной формой болезни в США[9]. Препарат «Майозайм» относится к одним из самых дорогих лекарств в мире, и годовой курс обходится от 100 до 300 тысяч долларов США в зависимости от возраста и веса пациента[10]. C 2013 года препарат зарегистрирован в РФ[11].
Прогноз[править | править код]
Прогноз данного редкого генетически детерминированного заболевания варьирует в зависимости от времени наступления и степени выраженности клинических симптомов. Без своевременного специфического лечения эта генетическая патология, особенно среди младенцев и маленьких детей, часто заканчивается летально.
См. также[править | править код]
- Гликогенозы
- Лизосомные болезни накопления
- Паренхиматозные дистрофии
- Помпе, Иоанн Кассианус
Примечания[править | править код]
- ↑ Pompe disease at NLM Genetics Home Reference (англ.)
- ↑ Pompe, J.C. Over idiopathische hypertrophie van het hart (нид.) // Nederlands Tijdschrift voor Geneeskunde (англ.)русск.. — 1932. — Bd. 76. — P. 304—312. (англ.)
- ↑ of Glycogen-Storage Disease Type II (Pompe Disease) 947870, раздел Genetics of Glycogen-Storage Disease Type II (Pompe Disease) (англ.) на сайте EMedicine
- ↑ Hers H. G. α-Glucosidase deficiency in generalized glycogen-storage disease (Pompe’s disease) (англ.) // Biochemical Journal. — 1963. — Vol. 86, no. 1. — P. 11—16. — PMID 13954110.
- ↑ la Marca G. Lysosomals // Physician’s Guide to the Diagnosis, Treatment, and Follow-Up of Inherited Metabolic Diseases / N. Blau, M. Duran, K. M. Gibson, C. D. Vici. — Springer Berlin Heidelberg, 2014. — P. 785-793. — ISBN 978-3-642-40336-1. (англ.)
- ↑ Ausems M.G., Verbiest J., Hermans M.P., et al. Frequency of glycogen storage disease type II in The Netherlands: implications for diagnosis and genetic counselling (англ.) // European Journal of Human Genetics (англ.)русск. : journal. — 1999. — September (vol. 7, no. 6). — P. 713—716. — doi:10.1038/sj.ejhg.5200367. — PMID 10482961. (англ.)
- ↑ Umapathysivam K., Hopwood J.J., Meikle P. J. Determination of acid alpha-glucosidase activity in blood spots as a diagnostic test for Pompe disease. Clin. Chem. 2001; 47; 1378—1383. (англ.)
- ↑ 1 2 3 Type II Glycogen Storage Disease (недоступная ссылка). The Association for Glycogen Storage Disease. Дата обращения 27 ноября 2014. Архивировано 23 июня 2012 года. (англ.)
- ↑ FDA Approves First Treatment for Pompe Disease (англ.). U.S. Food and Drug Administration (28 April 2006). Дата обращения 15 апреля 2015.
- ↑ Matthew Herper. The World’s Most Expensive Drugs (англ.). Forbes.com LLC (22 February 2010). Дата обращения 15 апреля 2015.
- ↑ Государственный реестр лекарственных средств. grls.rosminzdrav.ru. Дата обращения 14 января 2016.
Ссылки[править | править код]
- Русскоязычная пациентская группа о болезни Помпе и миопатиях
- Лизосомные болезни накопления
Источник
Ферменты, находящиеся во всех клетках ткани и в крови, выполняют катализаторов (ускорителей) всех биологических реакциях, происходящих в организме.
- клеточные
- секреторные
- экскреторные
Группы ферментов крови:
Секреторные ферменты синтезируются в печени и поступают непосредственно в кровь, где выполняют специфические функции. К таким ферментам относят церулоплазмин, липопротеиновую липазу, псевдохолинэстеразу. В случае, когда активность секреторных ферментов в крови снижается ниже нормы, возникает подозрение на наличие патологий печени.
Экскреторные ферменты синтезируются в органах пищеварения (поджелудочной железе, печени, желчных путях). Примерами таких ферментов могут служить α-амилаза, щелочная фосфатаза, липаза. При повышении активности экскреторных ферментов, возникают подозрения на наличие проблем с выделительной (экскреторной) системой.
Как уже было сказано выше, при исследовании крови определяют активность ферментов, единицами измерения которой (ME) принято считать количество фермента, которое в нормальных условиях катализирует (ускоряет) превращение 1 мкмоль субстрата за 1 минуту (мкмоль/л). Удивительным является факт того, что активность ферментов максимальна при температуре 37 °C. (активность ферментов очень чувствительная к изменению температуры).
Также по местонахождению их делят на неспецифические, которые ускоряют общие реакции, происходящие в большинстве тканей, и на органоспецифические (индикаторные), характерные для определенных типов тканей. Исследование ферментов проводится при первичном установлении диагноза, наблюдения за динамикой течения заболевания и прогноза выздоровления. Повышение активности ферментов выше нормы называют гиперферментемией, понижение ниже нормы – гипоферментемией, а нахождение ферментов, которых в норме быть не должно – дисферментемией.
Аминотрансферазы (АСТ, АЛТ) в крови
Аминотрансферазы это ферменты группы трансфераз (трансферазы это ферменты, которые катализируют реакции переноса функциональных групп от молекулы к молекуле), которые ускоряют реакции переноса аминогрупп от аминокислот к кетокислотам. Подобные ферменты широко распространены в организме человека, они содержатся в тканях сердца, печени, почек, легких и даже в скелете. Одними из ферментов-аминотрансфераз являются аспартатаминотрансфераза (АСТ) и аланинаминотрансфераза (АЛТ).
Аспартатаминотрансфераза (АСТ)
В диагностике измерение активности аспартатаминотрансфераз (будем обозначать просто АСТ) часто применяется для выявления повреждений миокарда при инфаркте миокарда. При инфаркте миокарда активность АСТ может быть повышена в 20 раз, при этом степень изменения активности указывает на патологическую массу миокарда. Зачастую увеличение активности АСТ в крови можно заметить до возможности обнаружения признаков инфаркта миокарда с помощью электрокардиографии (ЭКГ). При инфаркте миокарда активность АСТ в крови повышается через 5 — 36 часов, и снижается до нормы на 5 день.
Также АСТ повышен при патологиях печени, например остром гепатите, умеренное повышение наблюдается при механической желтухе (закупорке желчных путей камнями) и злокачественных опухолях.
Норма АСТ находится в пределах 10 — 30 МЕ/л.
Аланинаминотрансфераза (АЛТ) используется организмом для ускорения реакции переноса аминогрупп с аланина на α-кетоглутаровую кислоту. АЛТ распределена во всех тканях органов и скелета, максимального содержания она достигает в печени.
Норма аланинаминотрансферазы (АЛТ) находится в пределах 7 — 40 МЕ/л.
При инфаркте миокарда наряду с АСТ повышается и активность АЛТ, особенно в острой фазе (до 150 % от нормы). При патологии печени (например, острый гепатит) по сравнению с АСТ активность АЛТ повышена в более значительном диапазоне (до 1000 МЕ/л). Именно поэтому для ранней диагностики гепатита измерение активности АЛТ более информативно, чем АСТ.
Аланинаминотрансфераза (АЛТ)
| Превышение | Причины |
|---|---|
| в 2 раза | злоупотребление алкоголем |
| в 5 раз | стеатонекроз |
| в 10 раз | лекарственный холестатический гепатит, цирроз печени |
| в 20 раз | инфекционный мононуклеоз, холедозолитиаз |
| в 50 раз | поражение клеток печени лекарственными препаратами |
| в 100 раз | острый вирусный гепатит |
Физиологическое повышение активности бывает связано с приемом лекарственных препаратов, например эритроцимина, линкомицина, аскорбиновой кислоты, а также
Стоит упомянуть про коэффициент де Ритиса, который используют при такой диагностике: это отношение АСТ к АЛТ.
В норме коэффициент де Ритиса находится в пределах 0,91 – 1,75.
| Причина | Описание |
|---|---|
| инфаркт миокарда | преобладает активность АСТ (500% нормы) над АЛТ (150 % нормы), коэффициент де Ритиса больше 2. |
| острый гепатит | преобладает активность АЛТ (300 – 100 МЕ/л) над АСТ (150 – 1000 МЕ/л), коэффициент де Ритиса меньше 1. |
Снижение активности ниже нормы наблюдается при почечной недостаточности и во время беременности.
Общая лактатдегидрогеназа (ЛДГ) в крови
Норма активности лактатдегидрогеназы (ЛДГ) в крови находится в пределах 208 – 378 МЕ/л. Максимальная активность этого фермента обнаруживается в почках и сердечной мышце.
Различают физиологическое и патологическое повышение активности ЛДГ.
Физиологическое повышение ЛДГ возникает на фоне активных физических нагрузках и у женщин при беременности.
Лактатдегидрогеназа (ЛДГ)
Патологическое повышение активности ЛДГ в 2-4 раза выше нормы возникает при инфаркте миокарда, причем повышенной она остается в течение 10 суток. Небольшое повышение активности ЛДГ бывает при хронической сердечной недостаточности, миокардите и острой коронарной недостаточности. Также повышение активности ЛДГ возможно при инфаркте легких и легочной эмболии, но только при условии того, что уровень активности АСТ находится в норме, а концентрация билирубина повышена.
Лактатдегидрогеназа (ЛДГ)
Вирусные гепатиты также повышают активность ЛДГ, причем прямая зависимость степени повышения активности ЛДГ и тяжести гепатита.
Щелочная фосфатаза в крови
Щелочная фосфатаза
Щелочная фосфатаза катализирует реакции отсоединения фосфорной кислоты из соединений. Щелочная фосфатаза повышена при состояниях, связанных с поражением костей (переломы). Также повышение активности щелочной фосфатазы может свидетельствовать о наличии патологий печени, почек или при передозировке лекарственными препаратами (парацетамол, тетрациклин), приеме оральных контрацептивов, гиперпаратиреозе, цитомегаловирусной инфекции, тиреотоксикозе.
| Возраст | Активность, МЕ/л |
|---|---|
| Дети | 70 — 210 |
| Взрослые | 40 – 120 |
| Превышение | Причины |
|---|---|
| в 3 раза | острый вирусный гепатит, алкогольный гепатит |
| в 5 раз | цирроз печени, жировая дистрофия печени, инфекционный мононуклеоз |
| в 10 раз | постнекротический цирроз, холедохолитиаз |
| в 20 раз | лекарственный гепатит, опухоли печени, первичный билиарный цирроз |
Понижение активности щелочной фосфатазы возникает при выраженной анемии, гипофосфатемии, цинге и гипотиреозе.
Амилаза
Амилаза крови это фермент ускоряющий реакции превращения крахмала до простых олигосахаридов (моносахаридов и дисахаридов). В человеческом организме амилаза поступает в кровь из поджелудочной и слюнных желез, так как именно в них находится наибольшее количество данного фермента. Амилаза является важным ферментом, который, находясь в слюне, проявляет свою активность в самом начале процесса пищеварения – во рту человека.
Амилаза
- α-амилаза (альфа-амилаза)
- β-амилаза (бета-амилаза)
- γ-амилаза (гамма-амилаза)
Типы амилазы в крови:
α-амилаза
Альфа амилаза входит в список основных пищеварительных ферментов не только в организме человека и животных, но и в растениях, грибах и бактериях, причем в растениях этот фермент проявляет свою наибольшую активность на этапе прорастания семени.
Норма активности альфа амилазы в крови человека находится в пределах 25 – 220 МЕ/л.
Кровь человека содержит два типа α-амилазы: панкреатический (или P-тип) и слюнной (S-тип). α-амилаза панкреатического типа синтезируется клетками поджелудочной железы, а слюнная α-амилаза слюнного типа – клетками слюнных железа, причем в норме на долю панкреатического типа приходится около 30-50% (17-115 МЕ/Л) от общего количества α-амилазы, а слюнного примерно 60%.
Определение активности α-амилаза в крови имеет большое значение в диагностике патологий, например активность α-амилазы повышена в 2 — 30 раз при заболеваниях поджелудочной железы, например острого панкреатита, при этом повышается активность панкреатического типа α-амилазы, а активность слюнного типа α-амилазы не меняется. При остром приступе повышение активности α-амилазы (гиперамилаземия) происходит уже через 5 часов, достигает своего максимума через 12-24 часа и снижается до нормы на 3 – 6 сутки. Следует отметить, что для диагностики патологий поджелудочной железы определение активности α-амилазы в моче имеет большее информационное значение нежели в крови. К тому же, в некоторых случаях, острый панкреатит может возникать без повышения или снижения активности α-амилазы.
α-амилаза
Поэтому для большей точности в диагностике панкреатита исследуют изменения в активности α-амилазы вместе с изменениями концентрации креатинина в моче и крови, то есть рассчитывают амилазо-креатининовый клиренс по формуле, указанной ниже.
- АМ – алимаза в крови
- КрС – креатинин в сыворотке крови
- КрМ – креатинин в моче
(АМхКрС)/(КрМхАС), где
В норме амилазо-креатининовый клиренс должен быть не более 3, при повышении его значения более 3 диагностируют панкреатит (чем выше значение амилазо-креатининового клиренса, тем выше уровень панкреатического типа α-амилазы).
При наличии хронического панкреатита активность α-амилазы увеличивается в периоды обострения или при появлении препятствий для оттока панкреатического сока из-за воспаления, сдавливания протоков, отека головки поджелудочной железы. Понижение активности α-амилазы при хроническом панкреатите указывает на экзокринную недостаточность поджелудочной железы при атрофии тканей органа.
При гнойном панкреатите, сопровождающемся некрозом тканей поджелудочной железы, гиперамилаземия может отсутствовать.
Панкреатит
Однако повышение активности α-амилазы может быть вызвана не только приступами острого панкреатита, но и острым аппендицитом, язвой двенадцатиперстной кишки, перитонитом, кишечной непроходимостью, холециститом, диабетическом ацидозе, употреблении чрезмерного количества алкоголя, а также приемом таких лекарственных препаратов как кортикостеродов, сульфаниламидов, тетрациклина, морфина, пероральных констрацептивов. При наличии перечисленных заболеваний активность α-амилазы в крови может увеличиваться в 3-4 раза. Также активность панкреатической α-амилазы повышается по время беременности.
Повышение активности слюнной α-амилазы наблюдают при заболеваниях полости рта, например стоматите, паркинсонизме, а снижение при эмоциональных перегрузках и стрессе.
β-амилаза
Бета амилаза отсутствует в организме человека и животных. Находясь в бактериях, грибах и растениях, она расщепляет крахмал на простые сахара. Например, β-амилаза активно помогает созревающим фруктам становиться сладкими.
Липаза
Еще один фермент, определение которого имеет важное информационное значение при диагностике острого панкреатита это липаза. В периоды приступов острого панкреатита, липаза в крови может быть повышена в 200 раз.
Липаза
Норма активности липазы в крови находится в пределах от 0 до 190 МЕ/л.
Среди причин, вызывающих повышение активности липазы в крови можно выделить также перитонит, сахарный диабет, ожирение, подагра также прием барбитуратов.
Понижение активности липазы возникает при содержании в принимаемой пище большого количества жиров, а также при онкологических заболеваниях, за исключением рака поджелудочной железы.
При обострении хронического панкреатита активность липазы резко повышается до 200 раз в первые 12-24 часа, и сохраняет свое значение в течение 10-12 дней. Прогноз течения острого панкреатита считают неблагоприятным в случае, когда уровень липазы повысился в 10 раз, но не снизился до превышение нормы в 3 раза в первые дни.
Активность липазы не повышается при аппендиците, паротите и раке легких и других заболеваниях, при которых может повышаться уровень α-амилазы, поэтому совместное определение активности липазы и α-амилазы является обязательным при диагностике панкреатита. Для определения причины возникновения панкреатита используют липазо-амилазовый коэффициент, который равен отношению активности липазы к активности амилазы в крови. Например, если липазо-амилазовый коэффициент превышает значение 2, диагностируют острый алкогольный панкреатит.
Видео по теме
Это может быть полезным для Вас:
Источник


