Мпс анализ крови что это
Значительные достижения в изучении истинного генеза МПС и определение характера ферментативной недостаточности при большинстве известных форм стимулировали исследования по созданию тестов ранней диагностики этой группы заболеваний. Анализ литературы (Т. Т. Партош) показал не только перспективность развития этого направления, но и целесообразность использования предлагаемых диагностических приемов на практике.
Среди общепринятых скрининг-тестов различают spot-тесты (пробы с образованием пятна) и тесты на помутнение (основанные на реакции преципитации). Spot-тесты зависят от визуального сравнения метахроматических пятен мочи и стандартов хондроитинсульфата на бумаге и требуют от оценивающего человека способности тонко различать цвета окраски.
Метахроматический эффект возникает вследствие реакции кислотных функциональных групп полисахаридного полимера с основными группами краски. Однако некоторые вещества, отличающиеся от хондроитинсульфата, могут также давать метахромазию. Па преципитацию кислых гликозаминогликанов (КГАГ), лежащую в основе тестов на помутнение, влияет ионная концентрация и рН мочи.
Существует множество модификаций общепринятых тестов. Наиболее часто применяемые метахроматические тесты — это проба Берри с окраской толуидин-синим, проба с окраской алциан-синим, тест с MPS-бумагой (специальная бумага, пропитанная азуром А). Тестами на помутнение являются реакции преципитации с кислым альбумином, цетилтриметиламмонием бромидом (СТАВ), цетилпиридинхлоридом (СРС).
При сравнительной оценке скрининг-тестов на выявление избыточной экскреции кислых гликозаминогликанов учитывается простота метода, стоимость материалов, затрачиваемое время и, главное, надежность метода (процент ложноположительных и ложпоотрицательных результатов).
Ученые многих стран мира большое внимание уделяют проблеме скрининга мукополисахаридозов. Так, в США Rezvani и соавт. сравнили эффективность spot-теста (MPS-бумага), реакции преципитации с СТАВ и упрощенного теста с кислым альбумином. Каждым из этих тестов скринированы 13 детей с различными типами МПС и 96 детей, не больных МПС. При проведении скрининг-тестов использовались как разовые порции мочи, так и суточные.
Для подтверждения их надежности параллельно проводилось количественное определение КГАГ (методом карбозоловой реакции по Дише). Приведенные в таблице данные свидетельствуют о степени надежности скрининг-тестов. СТАВ-реактив дал наибольшее число ложноположительных результатов (42%). При пробе с MPS-бумагой ложноположительных результатов было меньше (34%). Тест с кислым альбумином дал всего 8% слабовыраженных ложноположительных результатов. Эти данные сходны с результатами исследования Carter.
Результаты проведения скрининг-тестов у 96 здоровых детей, %

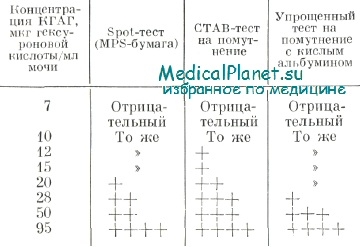
В таблице приведены данные по определению порога чувствительности использованных тестов. Наименьший обнаруженный уровень. КГЛГ мочи был при применении СТАВ-реактива: он составил 12 мкг гексуроновой кислоты/мл, при использовании MPS-бумаги — 20 мкг гексуроновой кислоты/мл, при реакции с кислым альбумином — 28 мкг гексуроновой кислоты/мл. Выраженные положительные результаты получаются при применении всех этих тестов, когда концентрация КГАГ в моче достигает 50 мкг гексуроновой кислоты/мл.
Верхняя граница КГЛГ в моче у обследованных детей, не больных МПС, была 38,3 мкг гексуроновой кислоты/мл. Следовательно, избыточная чувствительность этих тестов дает некоторый процент ложпоположительных результатов. Количество ложпоположительных результатов приблизительно соответствует предполагаемому порогу чувствительности. Все дети, больные МПС, дали резкоположительные результаты.
Таким образом, можно сделать вывод, что упрощенный тест на помутнение с кислым альбумином из перечисленных выше тестов является наиболее надежным для скрининга больных на МПС.
Преимущество теста с MPS-бумагой состоит в том, что он прост и занимает всего 3 мин времени, но этот метод часто дает ложноположительные результаты и дорого стоит.
Избыточная чувствительность СТАВ-теста приводит к ложноположительным результатам.
Число ложноположительных результатов при применении упрощенного теста с кислым альбумином было сходно с данными Carter и соавт.. Однако в отличие от исследований Carter и соавт. работы, проведенные Rezvani и соавт., не дали ложноотрицательпых результатов. Это могло быть частично вследствие малого числа больных МПС, подвергнутых обследованию (Carter с сотр. обследовал 54 больных мукополисахаридозом детей и 800 детей контрольной группы с умственной отсталостью, но без МПС), а также вследствие того, что, наряду с разовыми пробами исследовалась суточная моча.
Это говорит о том, что содержание КГАГ в разовых порциях мочи у больных МПС может быть иногда довольно низким, что является причиной ложноотрицательпых результатов. Таким образом, при подозрении на МПС и невозможности собрать суточную мочу разовые пробы необходимо исследовать у одного и того же больного несколько раз.
По данным Carter и соавт., spot-тест с окраской алциан-синим неспецифичен и дает большое число ложноположительных результатов. Наличие нескольких этапов при проведении этого теста делает его непригодным для целей массового скринирования. Spot-тест с толуидин-синим также недостаточно специфичен, однако 32% ложноотрицательных случаев у больных МПС превышает процент ложноотрицательных случаев в работах других авторов.
По мнению Rezvani и соавт., Carter и соавт., упрощенный тест на помутнение с кислым альбумином является наиболее подходящим для выявления больных МПС. Он отличается своей простотой и занимает мало времени.
Упрощенный тест па помутнение с кислым альбумином состоит в следующем: к 1,0 мл мочи добавляют 2,0 мл реактива кислого альбумина и 2 капли 5 н. соляной кислоты. Получающееся в результате помутнение оценивается по прошествии 10 мин: 1+, 2+, 3 + , 4+.
Чувствительность скрининг-тестов на выявление кислых гликозаминогликаное в моче

Pennok и соавт. в качестве скрининг-теста на МПС рекомендуют использовать тост на помутнение с цетилпиридинхлоридом (СРС) в цитратном буфере. При проведении данного теста к разовой пробе мочи добавляют 1,0 мл 0,1% раствора цетилпиридинхлорида в 0,1 М цитратном буфере. Результат оценивается через 30 мин и выражается в СРС-едипицах на 1 г креатинина (1 единица соответствует помутнению, которое дает раствор хондроитинсульфата с концентрацией 10 мг/л).
По мнению авторов, основные преимущества этого теста — простота и надежность. При тесте с СРС возможно применение разовых порций мочи, так как результаты даются в соотношении к креатинину. Он полезен при скрининге грудных детей, когда сбор суточной мочи наиболее труден, и облегчает раннюю диагностику МПС. Постановка диагноза МПС в раннем возрасте очень трудна еще и из-за того, что экскреция КГАГ в период новорожденности велика, достигает максимума на 2—3-й неделе жизни, уменьшаясь затем на протяжении детского возраста. Следовательно, для исключения ложноположительных результатов необходим повторный скрининг в раннем детском возрасте.
В Испании Sabater и соавт. провели скринирование на мукополисахаридоз с применением модифицированного теста Берри 15 000 новорожденных. Авторы рекомендуют систематический скрининг новорожденных на МПС и подчеркивают практическую важность его для выявления многих неизвестных моментов, которые существуют в отношении генетических, биохимических и физиологических аспектов этой группы заболеваний. Скрининг проводился следующим образом.
Полоски специальной фильтровальной бумаги выдавались родителям в родильном доме. Когда ребенку исполнялось 20 дней, родители прикладывали к мокрой пеленке эту полоску и затем отправляли ее по почте в специальном конверте. В лаборатории из этих полосок выбивались диски и производилась их окраска толуидин-синим. Если выделение КГАГ с мочой было избыточно, диски окрашивались в фиолетовый цвет.
Из 15 000 новорожденных на 20-й день у 103 получен положительный результат (0,68%), из их числа после запроса повторно получено 78 проб. При этом 5 проб от детей в возрасте 3 мес дали положительный результат. В шестимесячном возрасте производился новый контроль, который вновь дал 5 положительных результатов. В возрасте 1 года положительные результаты получены у 2 детей. Оба ребенка были клинически здоровы.
Параллельно производилось качественное определение в моче ферментов: b-галактозидазы, а-фукозидазы, арилсульфатазы. При этом обнаружено, что тесты становились отрицательными, когда появлялась ферментативная активность в моче. Это подтверждает возможность существования транзиторного дефицита ферментов, который сопровождается избыточной экскрецией КГАГ.
При диагностике МПС используются также исследования картины периферической крови и мазков костного мозга. При МПС отмечается наличие метахроматических грануляций в клетках крови и костного мозга. Однако в литературе диагностическая ценность этих исследований дискутируется.
Основываясь на опыте проведения проб у 84 больных МПС и 211 детей, составляющих контрольную группу, Szabo считает для целей скрининга пригодным использование модифицированного теста Берри с окраской толуидин-синим, но вместе с ним необходимо производить окраску толуидин-сипим и мазков крови. Применение для фиксации мазков раствора, состоящего из ацетата свинца, этанола, формалина и ледяной уксусной кислоты, а также обработка мазков тестикулярной гиалуропидазой увеличивают эффективность и специфичность метода. В !)4 % случаев получены результаты, подтверждающие диагноз МПС.
Все без исключения ложноположительные случаи после обработки тестикулярной гиалуропидазой оказались отрицательными. Из изложенного можно сделать следующие выводы:
1. Простые скрининг-тесты для выявления избыточной экскреции КГАГ необходимы, так как количественные методы определения гликозаминогликанурии очень сложны и требуют специально оснащенных лабораторий. Ранняя диагностика, осуществляемая при помощи скрининг-программ, важна для медико-генетического прогнозирования.
2. Для скрининга на мукополисахаридоз наиболее надежным является тест на помутнение с цетилпиридипхлорпдом в цитратном буфере, а также упрощенный тест с кислым альбумином.
3. Для исключения ложноположительных результатов в раннем возрасте необходим повторный скрининг, так как экскреция КГАГ в период новорожденности велика и достигает максимума на второй-третьей педеле жизни.
4. Целесообразно проведение селективного скрининга с целью обследования определенных контингентов детей: слабовидящих, с задержкой умственного развития, с патологией опорно-двигательного аппарата.
— Рекомендуем далее ознакомиться со статьей «Скрининг на цистинурию и гипероксалурию»
Оглавление темы «Нарушения обмена веществ»:
- Скрининг новорожденных на лейциноз — болезнь кленового сиропа
- Пример лейциноза у грудного ребенка
- Скрининг новорожденных на галактоземию
- Пример галактоземии у грудного ребенка
- Скрининг нарушений обмена триптофана, гиперлипопротеидемий
- Скрининг на мукополисахаридоз (МПС)
- Скрининг на цистинурию и гипероксалурию
- Программа выявления гетерозигот нарушений обмена веществ
- Принципы лечения нарушений обмена веществ
- Принципы лечебного питания при нарушениях обмена веществ
Источник
Диагноз МПС III устанавливается на основании совокупности клинических данных, результатов лабораторного исследования и молекулярно-генетического анализа.
Рекомендованы:
исследование спектра и количества экскретируемых гликозаминогликанов с мочой;
определение активности гепаран-N-сульфатазы, α-N-ацетил-D-глюкозаминидазы, гепаран ацетил-КоА:α-глюкозаминид-N-ацетилтрансферазы, N-ацетилглюкозамин-6-сульфатазы (в зависимости от подтипа) в культуре фибробластов, изолированных лейкоцитах;
проведение молекулярно-генетического исследования: выявление мутаций в генах
SGSH, NAGLU, HGSNAT, GNS (в зависимости от подтипа);
контроль биохимического анализа крови (определяют аланинаминотрансферазу (АЛТ),
аспартатаминотрансферазу (АСТ), общий и прямой билирубин, холестерин, триглицериды, креатинфосфокиназу (КФК), лактатдегидрогеназу (ЛДГ), кальций, фосфор,
щелочную фосфатазу (ЩФ));
контроль общего клинического анализа крови, мочи;
проведение ультразвукового исследования (УЗИ) органов брюшной полости, селезенки, почек;
проведение рентгенографии скелета;
проведение электромиографии (ЭМГ) и электронейромиографии (ЭНМГ);
проведение аудиометрии;
проведение исследования функции внешнего дыхания (ФВД);
проведение электроэнцефалографии (ЭЭГ);
проведение полисомнографии;
проведение электрокардиографии (ЭКГ) и эхокардиографии (Эхо-КГ);
проведение магнитно-резонансной томографии (МРТ) головного мозга, шейного отдела;
проведение компьютерной томографии (КТ) головного мозга.
Дифференциальная диагностика должна исключить другие виды мукополисахаридозов, муколипидозы, ганглиозидозы, альфа — маннозидоз, фукозидоз, множественную сульфатазную недостаточность.
В семьях, где есть больной ребенок, существует возможность проведения пренатальной и преимплантационной диагностики. Пренатальная диагностика возможна путем измерения активности ферментов на 9-11 неделе беременности и/или определения спектра ГАГ в амниотической жидкости на 20-22 неделе беременности.
Обязательно нужно знать подтип синдрома Санфилиппо (A, B, C или D), так как каждый из них требует различных тестов, и при внутриутробной диагностике невозможно провести все четыре типа тестов одновременно. Важно проконсультироваться со специалистом на ранних сроках беременности, если вы хотите сделать такие тесты. Для диагностики МПС до рождения ребенка используются амниоцентез и обследование хорионических ворсинок.
Диагноз МПС IV устанавливается на основании совокупности клинических данных, результатов лабораторного исследования и молекулярно -генетического анализа. В отличие от других типов, мукополисахаридозов IV тип характеризуется отсутствием снижения интеллекта, помутнения роговицы, гепатоспленомегалии.
Рекомендованы:
анализ количества и спектра гликозаминогликанов, экскретируемых с мочой;
исследование активности галактозамин-6-сульфат-сульфатазы (в случае МПС IVA),
β-галактозидазы (в случае МПС IVB) в культуре фибробластов, изолированных лейкоцитов, либо в пятнах крови, высушенных на фильтровальной бумаге;
молекулярно-генетическое исследование: выявление мутаций в генах GALNS
(для МПС IVA) и GBS (для МПС IVB);
проведение ультразвукового исследования (УЗИ) органов брюшной полости, селезенки, почек;
проведение рентгенографии скелета;
проведение электромиографии (ЭМГ) и электронейромиографии (ЭНМГ);
проведение аудиометрии;
проведение исследования функции внешнего дыхания (ФВД);
проведение электроэнцефалографии (ЭЭГ);
проведение полисомнографии;
проведение электрокардиографии (ЭКГ) и эхокардиографии (Эхо — КГ);
проведение магнитно-резонансной томографии (МРТ) головного мозга,
шейного отдела;
проведение компьютерной томографии (КТ) головного мозга.
Дифференциальная диагностика проводится с различными вариантами нанизма, наследственными заболеваниями скелета, сопровождающимися спондилоэпифизарными нарушениями.
В семьях, где есть больной ребенок, существует возможность проведения пренатальной и преимплантационной диагностики. Пренатальная диагностика возможна путем измерения активности ферментов на 9-11 неделе беременности. Для семей с известным генотипом возможно проведение ДНК-диагностики.
Диагноз мукополисахаридоза VII основывается на клинических проявлениях, данных рентгенологического исследования, определении экскреции с мочой гликозаминогликанов, исследовании активности специфических ферментов культуре клеток (фибробластах кожи и лейкоцитах), амниотической жидкости (антенатальная диагностика).
Лабораторная диагностика
Для подтверждения диагноза мукополисахаридоза VII проводят определение уровня экскреции глюкозамигликанов мочи и измерение активности бета-глюкуронидазы. В случае мукополисахаридоза VII возрастает суммарная экскреция гликозаминогликанов в моче и наблюдается гиперэкскреция дерматансульфата и гепарансульфата. Активность бета-глюкуронидазы измеряют в лейкоцитах или культуре кожных фибробластов с использованием искусственного флюорогенного субстрата.
Пренатальная диагностика возможна путём измерения активности бета-глюкуронидазы в биоптате ворсин хориона на 9-11-й неделе беременности и/или определения спектра гликозаминогликанов в амниотической жидкости на 20-22-й неделе беременности. Для семей с известным генотипом возможно проведение ДНК-диагностики на ранних сроках беременности.
Дифференциальная диагностика
Дифференциальная диагностика проводится как внутри группы мукополисахаридозов, так и с другими лизосомными болезнями накопления: муколипидозами, галактосиалидозом, сиалидозом, маннозидозом, фукозидозом, GM1-ганглиозидозом.
Источник

