Генетический анализ крови при раке молочной железы

Информация об исследовании
Состав генетического комплекса:
- Рак молочной железы 1 (BRCA1). Полиморфизм: 5382InsC
- Рак молочной железы 1 (BRCA1). Полиморфизм: 4153DelA
- Рак молочной железы 2 (BRCA2). Полиморфизм: 6174DelT
- Рак молочной железы 1 BRCA1: 185delAG
- Рак молочной железы 1 BRCA1: 3819delGTAAA
- Рак молочной железы 1 BRCA1: 3875delGTCT
- Рак молочной железы 1 BRCA1: 300 T>G (Cys61Gly)
- Рак молочной железы 1 BRCA1: 2080delA
Рак молочной железы – самая распространённая форма рака у женщин. Так, в России, из всех женщин, заболевших раком, каждая пятая (21%) имеет именно эту патологию – рак молочной железы.
Каждый год страшный диагноз слышат более 65 тысяч женщин, из них уходят из жизни более 22 тысяч. Хотя полностью избавиться от болезни на ранних стадиях возможно в 94% случаев. В этот комплекс входит определение мутаций в генах BRCA1 и BRCA2.
Рак молочной железы и наследственность:
Рак молочной железы в семейной истории болезни вот уже многие годы считается фактором риска. Около ста лет назад были описаны случаи семейного рака молочной железы, передающиеся из поколения в поколение. В некоторых семьях болеют только раком груди; в других появляются и другие виды рака.
Около 10-15% случаев заболеваний раком молочной железы – наследственные. Риск заболеть раком груди для женщины, мать или сестра которой болели этой болезнью, в 1,5-3 раза выше по сравнению с женщинами, чьи ближайшие родственники не болели раком молочной железы.
Рак молочной железы во всем мире считается наиболее исследованным онкологическим заболеванием. Каждый год появляется новая информация о природе этого онкологического заболевания и разрабатываются методики лечения.
Гены BRCA1 и BRCA2:
Еще в начале 90-х годов BRCA1 и BRCA2 были идентифицированы как гены предрасположенности к раку молочной железы и раку яичников.
Наследственные мутации в генах BRCA1 и BRCA2 приводят к возрастающему в течение жизни риску развития рака груди. Оба этих гена имеют отношение к обеспечению стабильности генома, а точнее, в механизме гомологичной рекомбинации для репарации двухцепочечной ДНК.
Помимо рака молочной железы, мутации в гене BRCA1 проявляются при раке яичников, причем оба типа опухолей развиваются в более раннем возрасте, чем при ненаследственном РМЖ.
BRCA1-ассоциированные опухоли в целом связаны с неблагоприятным прогнозом для пациентки, поскольку чаще всего относятся к трижды негативному РМЖ. Этот подтип назван так из-за отсутствия в клетках опухоли экспрессии сразу трёх генов — HER2, рецепторов эстрогенов и прогестерона, поэтому и лечение, основанное на взаимодействии лекарств с этими рецепторами, невозможно.
Ген BRCA2 также вовлечен в процессы репарации ДНК и поддержание стабильности генома, — отчасти вместе с комплексом BRCA1, отчасти через взаимодействие с другими молекулами.
Мутации, характерные для определенных сообществ и географических групп, описаны также и для жителей нашей страны. Так, в России мутации BRCA1 представлены в основном пятью вариациями, 80% из которых — 5382insC. Мутации генов BRCA1 и BRCA2 приводят к хромосомной нестабильности и злокачественной трансформации клеток молочной железы, яичников и других органов.
Риск заболевания раком груди у женщин с мутацией генов BRCA1 и BRCA2:
У женщин – носительниц мутаций в одном из генов BRCA1 и BRCA2, риск заболеть раком молочной железы и раком яичников (реже – другими видами рака) выше, чем у других.
Следует подчеркнуть, что степень риска заболеть раком груди меняется в зависимости от семейного анамнеза. Степень риска повторно заболеть раком груди у женщины – носительницы мутации, уже переболевшей раком груди, составляет 50%. Риск заболеть раком яичников у носительниц мутации в гене BRCA1 составляет 16-63%, а у носительниц мутации в гене BRCA2 – 16-27%.
Показания к назначению исследования:
- В рамках программы скрининга и профилактики рака молочной железы с целью выявления вероятности наследственной предрасположенности.
- Женщинам, у родственников которых была обнаружена мутация в одном из генов.
- Женщинам с раком молочной железы или яичников в семейном анамнезе.
- Женщинам, переболевшим раком груди до 50 лет или переболевшим двусторонним раком груди.
- Женщинам, переболевшим раком яичников.
Источник

— Реклама —

Рак груди может встречаться в нескольких поколениях одной семьи: у бабушки, мамы и дочери диагностируется злокачественная опухоль. Такие формы рака называют наследственными, и по мере развития онкогенетики стала понятна причина их возникновения. В 90-х годах прошлого века были открыты гены-онкосупрессоры, несущие информацию о белках, блокирующих процессы злокачественной трансформации клеток. Сейчас науке известно множество генов с такой функцией: BRCA1, BRCA2, CHEK2, CDH1, PTEN, STK11, но наибольшее практические значение получили BRCA1 и BRCA2.
Что это за загадочные аббревиатуры: BRCA1 и BRCA2?
Это сокращение английского словосочетания Breast Сancer, которое переводится как рак груди. Мутации в генах BRCA1/BRCA2 – причина возникновения рака молочной железы у 5–10% женщин. Их роль в развитие онкологических процессов была открыта в 1994 году.
Гены BRCA1/BRCA2 кодируют белки, выполняющие в клетке функции супрессоров опухолевого роста. Они участвуют в восстановлении разрывов нитей молекул ДНК и участвуют в поддержании стабильности генома. Нарушение их работы ведет к нарастанию ошибок в ходе репарации ДНК. На клетки с поврежденным генетическим материалом действуют белки-регуляторы клеточного цикла и «отправляют» их в апоптоз – программируемую клеточную гибель. Однако, ошибки репарации вызывают нестабильность клеточного генома, что, в свою очередь, приводит к инактивации белков-регуляторов. Результат – приобретение клеткой способности к бесконечному делению и отсутствие у нее реакции на механизмы контроля – ключевой момент онкогенеза.
В моей семье были случаи рака молочной железы. Можно определить грозит ли мне наследственная форма РМЖ?

Да, можно. Для этого надо сдать генетический анализ в диагностической лаборатории. У вас возьмут образец венозной крови или соскоб со слизистой щеки и с помощью методов молекулярной диагностики изучат генетический материал ваших клеток. Если мутация есть, то результат анализа будет положителен. Однако тест рекомендуют проводить не всем людям, имеющим родственников с РМЖ. Основанием для назначения анализа здоровым женщинам служат следующие условия:
- двое и более ваших родственников болели раком груди, включая мужчин (отец, брат, дед);
- даже одному вашему родственнику диагноза РМЖ или рака яичников был поставлен ранее 40 лет;
- в вашей семье были случаи рака сразу обеих молочных желез;
- ваш возраст старше 20 лет.
У меня диагностирован рак молочной железы и врач рекомендовал сделать анализ на мутацию в генах BRCA1/BRCA2. Зачем?
Как правило, врачи направляют на генетический анализ и пациенток с уже диагностированным раком груди. На первый взгляд кажется, что в анализе нет смысла, ведь рак уже возник. Однако информация о наличии или отсутствии мутации помогает онкологу спланировать лечение и подобрать оптимальную для каждой формы болезни терапию, так как у наследственного РМЖ есть свои особенности течения.
Показаниями для выполнения теста служат:
- злокачественная опухоль, возникшая в молодом возрасте (до 35 лет);
- тройной негативный РМЖ;
- развитие рака одновременно в груди и яичниках;
- множественные опухоли.
Результат анализа на мутации в генах BRCA1/BRCA2 положительный. Что это значит?


Положительный анализ означает, что вы носитель мутации, которая повышает индивидуальный риск развития РМЖ до 40–80%, а также рака яичников до 40%. Нарушения структуры генов могут быть переданы потомству любого пола с вероятностью 50%. Ваши родные братья и сестры также могут быть носителями этой мутации с вероятностью 50%.
У мужчин мутация в генах BRCA1/BRCA2 также повышает риск возникновения рака груди и предстательной железы.
Но это не значит, что у вас обязательно разовьется рак молочной железы или яичников. Носители мутации могут прожить с ней всю жизнь и не заболеть РМЖ.
Анализ показал наличие мутации. Что делать в этом случае?
Вы можете предпринять ряд мер, которые позволят в определенной степени контролировать процесс развития болезни.
- Носители мутации должны проходить регулярное обследование груди начиная с 20 лет. «Золотым стандартом» в этом случае будет – МРТ молочных желез с контрастированием и УЗИ. Важная деталь: обследования проводятся поочередно, интервал между ними – 6 месяцев. То есть, сначала выполняется МРТ, а через полгода УЗИ. После 40 лет добавляется ежегодная маммография.
- Наличие мутации также говорит о том, что внешние факторы, вызывающие рак, могут оказать на вас большее действие, чем у людей без нее. Поэтому особенно важно изменить свой образ жизни: следить за весом, избегать неоправданной гормонотерапии, избыточного пребывания на солнце, облучения грудной области. Интересно, что ранние роды – доказанный способ защиты от РМЖ, не эффективны при носительстве мутантного гена.
- Один из методов профилактики – превентивная химиотерапия – применение препаратов, блокирующих рецепторы эстрогена в молочной железе, и исключающих избыточное деление ее клеток под действием гормона.
- Самый радикальный способ профилактики наследственного рака груди – превентивное удаление здоровых молочных желез, а также яичников. Мнения врачей по поводу эффективности этого метода неоднозначны. Удаляя ткани железы, мы устраняем «субстрат» для развития раковой опухоли, но при этом наносим женщине сильную психологическую травму. К тому же операция не исключает возникновение рака на 100%.
Результат анализа на мутации в генах BRCA1/BRCA2 отрицательный. Это значит, что у меня не будет рака молочной железы?

Нет. Это значит, что вы не носитель мутантного аллеля, несмотря на то, что ваши ближайшие родственники болели раком груди. Ваш риск заболеть РМЖ не выше среднего в популяции и равен 3–10%. Но это не значит, что можно не посещать маммолога и не проходить регулярную маммографию после 40 лет.
Правда, следует помнить о ложноотрицательных результатах. Они маловероятны, но возможны. Например, у женщины отягощенная наследственность по РМЖ и возникший в молодом возрасте рак груди, но анализ на мутации отрицательный. В этом случае возникают сомнения в точности полученных данных. Такая ситуация становится возможной, если РМЖ возникает из-за пока некартированной и соответственно неопределяемой мутации.
К сожалению, мутация в генах, повышающая вероятность развития раковой опухоли, остается с человеком на всю жизнь. Но предупрежден, значит вооружен. Внимательное отношение к своему здоровью, изменение образа жизни и регулярные профилактические обследования позволят держать возникновение опухоли под контролем.
Анастасия Хомякова, врач-диагност
Иллюстрации: Юлия Прососова
Источник
Одним из самых частых видов семейных опухолей является наследственный рак молочной железы (РМЖ), он составляет 5-10% от всех случаев злокачественного поражения молочных желез. Часто наследственный РМЖ связан с высоким риском развития рака яичника (РЯ). Как правило, в научной и медицинской литературе используют единый термин «синдром РМЖ/РЯ» (breast-ovarian cancer syndrome). Причем, при опухолевых заболеваниях яичника доля наследственного рака даже выше, чем при РМЖ: 10-20% случаев РЯ обусловлены присутствием наследственного генетического дефекта.
С предрасположенностью к возникновению синдрома РМЖ/РЯ связано присутствие у таких пациентов мутаций в генах BRCA1 или BRCA2. Мутации являются наследственными – то есть, буквально в каждой клетке организма такого человека есть повреждение, которое передалось ему по наследству. Вероятность возникновения злокачественного новообразования у пациентов с мутациями BRCA1 или BRCA2 к 70 годам достигает 80%.
Гены BRCA1 и BRCA2 играют ключевую роль в поддержании целостности генома, в частности в процессах репарации (восстановления) ДНК. Мутации, затрагивающие эти гены, как правило приводят к синтезу укороченного, неправильного белка. Такой белок не может правильно выполнять свои функции – «следить» за стабильностью всего генетического материала клетки.
Однако, в каждой клетке присутствует две копии каждого гена — от мамы и от папы, поэтому вторая копия может компенсировать нарушение работы клеточных систем. Но вероятность выхода ее из строя также очень высока. При нарушении процессов восстановления ДНК в клетках начинают накапливаться и другие изменения, которые, в свою очередь, могут привести к злокачественной трансформации и росту опухоли.
Определение генетической предрасположенности к онкологическим заболеваниям:
На базе лаборатории молекулярной онкологии НМИЦ онкологии им. Н.Н. Петрова применяется проведение поэтапного анализа для пациентов:
- сначала исследуется присутствие самых частых мутаций (4 мутации)
- при отсутствии таковых и клинической необходимости возможно проведение расширенного анализа (8 мутаций) и/или анализа полной последовательности генов BRCA1 и BRCA2.
С марта 2020 г. лаборатория молекулярной онкологии НМИЦ онкологии им. Н.Н. Петрова, возглавляемая членом-корреспондентом РАН, профессором Евгением Наумовичем Имянитовым, включена в систему ОМС (обязательного медицинского страхования).
На данный момент известно более 2 000 вариантов патогенных мутаций в генах BRCA1 и BRCA2. Кроме того, данные гены являются довольно большими – 24 и 27 экзонов соответственно. Поэтому полный анализ последовательностей генов BRCA1 и BRCA2 является трудоемким, дорогостоящим и длительным по времени процессом.
Однако для некоторых национальностей характерен ограниченный спектр значимых мутаций (т.н. «эффект основателя»). Так в популяции российских пациентов славянского происхождения до 90% обнаруживаемых патогенных вариантов BRCA1 представлены всего тремя мутациями: 5382insC, 4153delA, 185delAG. Этот факт позволяет значительно ускорить генетическое тестирование пациентов с признаками наследственного РМЖ/РЯ.
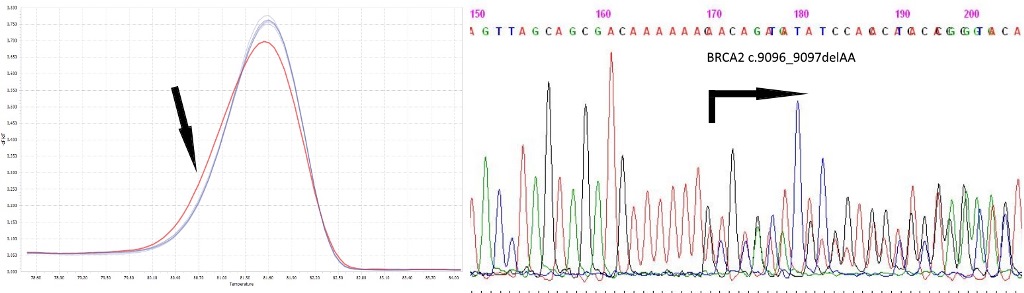
Анализ последовательности гена BRCA2, выявление мутации c.9096_9097delAA
В каких случаях нужно сдать анализ на мутации BRCA1 и BRCA2?
Национальная онкологическая сеть – National Comprehensive Cancer Network (NCCN) рекомендует направлять на генетическое исследование следующих пациентов:
- Пациенты до 45 лет с диагнозом рак молочной железы
- Пациенты в возрасте до 50 лет с РМЖ, если в семье есть хотя бы один близкий кровный родственник с таким диагнозом
- Также в том случае, если у пациента до 50 лет с РМЖ семейная онкологическая история неизвестна
- Если в возрасте до 50 лет диагностировано множественное поражение молочных желез
- Пациенты с РМЖ в возрасте до 60 лет — если по результатам гистологического исследования опухоль является трижды-негативной (отсутствует экспрессия маркеров ER, PR, HER2).
- При наличии диагноза рак молочной железы в любом возрасте — если присутствует хотя бы один из следующих признаков:
- не менее 1 близкой родственницы с РМЖ в возрасте менее 50 лет;
- не менее 2 близких родственниц с РМЖ в любом возрасте;
- не менее 1 близкой родственницы с РЯ;
- наличие не менее 2 близких родственников с раком поджелудочной железы и/или раком предстательной железы;
- наличие родственника-мужчины с раком грудной железы;
- принадлежность к популяции с высокой частотой наследственных мутаций (например, евреи Ашкенази);
- Все пациенты с диагностированным раком яичников.
- Если диагностирован рак молочной железы у мужчины.
- Если диагностирован рак простаты (с индексом по шкале Глисона >7) при наличии не менее одного родственника с РЯ или РМЖ в возрасте менее 50 лет или при наличии не менее двух родственников с РМЖ, раком поджелудочной железы или раком простаты.
- Если диагностирован рак поджелудочной железы при наличии не менее одного родственника с РЯ или РМЖ в возрасте менее 50 лет или при наличии не менее двух родственников с РМЖ, раком поджелудочной железы или раком простаты.
- Если рак поджелудочной железы диагностирован у уиндивидуума, принадлежащего к этносу евреев Ашкенази.
- Если у родственника обнаружена мутация BRCA1 или BRCA2
Выполнение молекулярно-генетического анализа должно сопровождаться генетическим консультированием, в ходе которого обсуждаются содержание, смысл и последствия тестирования; значение позитивного, негативного и неинформативного результатов; технические ограничения предлагаемого теста; необходимость информировать родственников в случае обнаружения наследственной мутации; особенности скрининга и профилактики опухолей у носителей мутаций и др.
Как сдать анализ на мутации BRCA1 и BRCA2?
Материалом для анализа является кровь. Для генетических исследований используют пробирки с ЭДТА (фиолетовая крышка). Сдать кровь можно в лаборатории НМИЦ или привезти из любой другой лаборатории. Кровь хранится при комнатной температуре до 7 дней.
Особая подготовка к исследованию не нужна, на результаты исследования не влияют приемы пищи, прием лекарств, введение контрастных веществ и пр.
Пересдавать анализ через некоторое время или после лечения не потребуется. Наследственная мутация не может исчезнуть или появиться в течение жизни или после полученного лечения.
Что делать, если у женщины обнаружена мутация BRCA1 или BRCA2?
Для носителей патогенных мутаций разработан комплекс мероприятий по ранней диагностике, профилактике и терапии новообразований молочной железы и рака яичников. Если среди здоровых женщин своевременно выявить тех, у кого имеется генный дефект, есть возможность диагностировать развитие заболевания на ранних стадиях.
Исследователями были выявлены особенности лекарственной чувствительности BRCA-ассоциированных опухолей. Они хорошо реагируют на некоторые цитостатические препараты, и лечение может быть весьма успешным.
Для здоровых носителей BRCA-мутаций рекомендовано:
- Ежемесячное самообследование с 18 лет
- Клиническое обследование молочных желез (маммография или магнитно-резонансная томография) с 25 лет.
- Мужчинам-носителям мутации в генах BRCA1/2 рекомендовано проведение ежегодного клинического обследования грудных желез начиная с 35-летнего возраста. С 40 лет целесообразно выполнение скринингового обследования предстательной железы.
- Проведение дерматологического и офтальмологического осмотров c целью ранней диагностики меланомы.
Как предрасположенность к РМЖ и РЯ передается по наследству.
Часто у носителей мутаций BRCA1/BRCA2 возникает вопрос – всем ли детям она передалась и какие генетические причины появления наследственной формы РМЖ? Шансы передать повреждённый ген потомству составляют 50%.
Заболевание одинаково наследуется, как мальчиками, так и девочками. Ген, связанный с развитием рака молочной железы и рака яичников, расположен не на половых хромосомах, поэтому вероятность носительства мутации не зависит от пола ребенка.
Если мутация в нескольких поколениях передавалась через мужчин, очень сложно проводить анализ родословных, так как мужчины довольно редко болеют РМЖ даже при наличии генного дефекта.
Например: носителями были дедушка и отец пациентки, и у них заболевание не проявилось. На вопрос, были ли случаи онкологических заболеваний в семье, такая пациентка ответит отрицательно. При отсутствии других клинических признаков наследственных опухолей (ранний возраст/множественность опухолей), наследственная составляющая заболевания может быть не учтена.
При обнаружении мутации BRCA1 или BRCA2 всем кровным родственникам рекомендуется также пройти тестирование.
Почему при генетическом исследовании важно учитывать этнические корни?
Для многих этнических групп характерен свой набор частых мутаций. Национальные корни обследуемого необходимо учитывать при выборе глубины исследования.
Учеными было доказано, что для некоторых национальностей характерен ограниченный спектр значимых мутаций (т.н. «эффект основателя»). Так в популяции российских пациентов славянского происхождения до 90% обнаруживаемых патогенных вариантов BRCA1 представлены всего тремя мутациями: 5382insC, 4153delA, 185delAG. Этот факт позволяет значительно ускорить генетическое тестирование пациентов с признаками наследственного РМЖ/РЯ.
И, в заключение, наглядная инфографика «Синдром наследственного рака молочной железы и яичников». Автор — Кулигина Екатерина Шотовна, к.б.н., старший научный сотрудник Научной лаборатории молекулярной онкологии ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России.

Источник
