Анализ крови риа что это
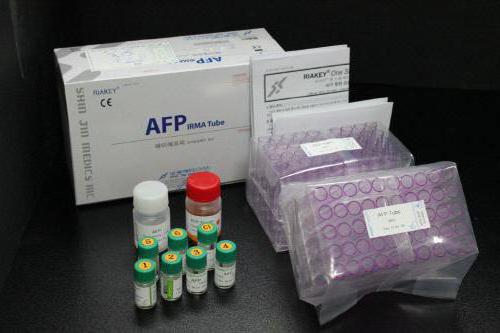
Современная медицина обладает методами специфического диагностирования, которые дают возможность устанавливать этиологию заболеваний у людей на основании определения возбудителя, генетически чужеродных веществ, что стимулируют иммунную реакцию, нуклеиновых кислот, а также сдвигов аллергического и иммунного характера, которые происходят из-за его действия. Сегодня в иммунологии и вирусологии широко применяется РИА, то есть радиоиммунный анализ, цели постановки, компоненты, ход, учеткоторого, мы рассмотрим в данной статье. Этот анализ способен определять антигены в результате их взаимодействия с антителами.

Определение
РИА представляет собой такой метод диагностирования биологически активных веществ в жидкостях, в основе которого лежат реакции антигенов с антителами при применении меченых радионуклидами аналогичных им веществ, которые имеют особые системы связывания. После их взаимодействия образуется иммунный комплекс, который отделяют и изучают его радиоактивность. Известно, что радиоиммунный анализ проводится при помощи стандартных наборов реагентов.
Каждый реагент способен определить концентрацию одного конкретного вещества. Биологическая жидкость, взятая у человека, смешивается с реагентом, по прошествии периода инкубации происходит разделение свободного и связанного радиоактивного вещества, далее проводится радиометрия и расчет результатов. Для метки веществ применяют изотоп йода. Его метят и добавляют в определенном количестве.

Применение
Радиоиммунный анализ применение имеет широкое в медицине и микробиологии. С его помощью проводится диагностика сердечных и сосудистых заболеваний, болезней эндокринной и иных систем организма. Также часто РИА используются для выявления причины бесплодия, патологии развития плода. В онкологии этот анализ проводят с целью определения маркеров новообразований, чтобы иметь возможность контролировать эффективность лечения. В иммунологии РИА применяется для исследования в крови наличия иммуноглобулинов, ферментов, белков и так далее. Сегодня данный анализ позволяет выявлять концентрацию различных гормонов до миллионной части одного грамма. Таким образом, радиоиммунный анализ кровишироко применяется в кардиологии, онкологии, эндокринологии, гинекологии и вирусологии.

Методы РИА
Принято различать несколько методов анализа, в зависимости от характера реакции:
- Неконкурентный метод характеризуется такими компонентами реакции, как стандартный и определяемый антигены, буферный раствор, антитела, что помечены изотопом, определенные антитела, что связываются на сорбенте. К антителам добавляют антиген, который исследуется. После инкубации появляются комплексы антиген-антитело, сорбент омывают, добавляют помеченные антитела, что вступают в связь с антигеном в составе комплекса. Радиоактивность зависит от концентрации антигена, что исследуется.
- Конкурентный радиоиммунный анализ обуславливается конкуренцией антигена. Здесь имеются такие компоненты реакции, как контрольный и определяемый антигены, буферный раствор, определенные антитела, что связываются на сорбенте, а также антиген, помеченный изотопом. Диагностирование начинается с ввода антигена, что исследуется. На сорбенте образуется комплекс антиген-антитело. Дальше омывается сорбент, и вводят помеченный антиген. При этом он вступает в связь с антителом. При помощи счетчиков измеряют реакцию и величину радиоактивности. Она будет в обратной пропорции относительно количества антигена в пробе.
- Непрямой метод является самым распространенным. В этом случае радиоиммунный анализ компоненты реакции имеет такие, как контрольная и исследуемая сыворотка, антигены или антитела, которые связаны на сорбенте, антитела, помеченные изотопами, растворы буферов. Антитела или антигены, что диагностируются, вступают в реакцию с антигенами или антителами, которые связаны на сорбенте. Потом удаляют инкубат, вводят помеченные антитела, что вступают в связь с комплексами антиген-антитело.
Методика проведения анализа
Так, радиоиммунный анализ проводится при помощи особых реагентов. Наборы стандартные, поэтому какие-либо погрешности или нарушения не допускаются. Результаты диагностики получаются достоверными. Анализ проводят утром, для этого берут у человека венозную кровь. В лаборатории от крови отделяют сыворотку, которая будет применяться для РИА. Эту сыворотку смешивают с реагентами. Полученная смесь проходит инкубацию при заданной температуре в термостате.
В полученной смеси разделяют свободные и связанные изотопы. После этого полученный материал исследуется, и просчитываются результаты. Механизм радиоиммунного анализа имеет несколько вариантов. Методика, что описана выше, является РИА жидкофазным, так как все компоненты имеют жидкое состояние. Есть РИА и твердофазный, где антитела кладут в носитель, который не растворяется в жидкости.
Доступность диагностики
Использование этого метода диагностики в медицине с каждым годом становится все популярнее. В последнее время радиоиммунный анализ становится стандартным методом диагностики, который может быть назначен врачом при постановке окончательного диагноза. Долгое время этот вид анализа проводился только в лабораториях, сегодня он стал обычным методом исследования. Но РИА требует применения дорогостоящего оборудования (гамма-счетчиков), а наборы реагентов имеют короткий эксплуатационный срок. Все это является основным недостатком такого анализа, что определяют его дорогую стоимость.
Кроме того, в последнее время РИА стали вытеснять более современные методы исследования, которые не требуют взаимодействия с изотопами. К таким относится иммуноферментный анализ. Таким образом, РИА является желанным во многих клиниках. В больших городах и центрах диагностики он давно используется, но в обычных больницах маленьких городов этот анализ практически не применяется из-за своей дороговизны.

Достоинства РИА
Радиоиммунный анализ имеет множество достоинств. Он достаточно специфичен и имеет высокую чувствительность, что позволяет определить наличие биологически активных веществ в невероятно малых количествах. Проводится этот анализ очень просто, от человека требуется только сдать венозную кровь. Результаты теста получаются точными на все 100% и готовы уже на следующий день. Также РИА с легкостью можно автоматизировать. Таким образом, этот анализ позволяет выявлять белки, которые представляют собой продукты жизнедеятельности инфекционных бактерий, что свидетельствует о наличии инфекции в организме.
Диагностика в вирусологии
Самым перспективным РИА является для вирусологии, поскольку позволяет в короткие сроки выявить вирусных возбудителей. Связано это с тем, что в последнее время растет число заболеваемости различными инфекциями, которые распространяются с большой скоростью, вызывая смертность среди людей. Особенно это касается стран, которые не имеют высокого социального и экономического развития (страны Дальнего Востока), здесь просто незаменим радиоиммунный анализ. Микробиология также применяет этот метод диагностики для выявления инфекционных болезней, которые вызывают патогенные бактерии. Например, РИА широко используют для выявления брюшного тифа. В первые дни недуга до назначения лечения необходимо проведение исследования кала и рвотных масс. Однако результаты диагностирования будут получены через длительное время. Здесь на помощь приходит РИА, анализ позволяет в короткий срок выявить возбудителя заболевания. Человек сдает кровь, на следующий день уже готовы результаты исследования. Этот анализ помогает в постановке точного диагноза.
Итоги
Радиоиммунный анализ является на данный момент одним из самых чувствительных методов диагностирования. Он используется для анализа любого вещества, против которого можно получить антитела. Этот метод дает возможность сделать множество проб в самом маленьком объеме исследуемой жидкости, а также в кратчайшие сроки провести учет результатов, так как он может быть полностью автоматизирован. Этот анализ был разработан в пятидесятых годах прошлого столетия Соломоном Берсоном. Через тридцать лет он получил широкое распространение. На сегодняшний день РИА нет стопроцентной альтернативы, так как анализ имеет высокую чувствительность. РИА используют в различных отраслях медицины, а также в микробиологии и вирусологии.

Напоследок
Использование метода в вирусологии очень актуально сегодня, так как дает возможность исследовать распространение инфекций, поставить точный диагноз и назначить специфическое лечение. Особенно эта проблема актуальна для стран, которые имеют низкий уровень экономики и социального развития. Также этот анализ позволяет выявлять количество гормонов и ферментов в организме человека. Для того чтобы получить достоверные результаты, исследуемому необходимо только сдать кровь на анализ. Медицина не стоит на месте, наряду с радиоиммунным анализом появляются новые методы исследования, но РИА продолжает оставаться одним из ведущих в медицинской диагностике.
Источник
В 1956 г. они впервые обнаружили у больных, леченных инсулином, непреципитирующие антитела, способные связывать 131I-инсулин. Затем эта научная группа показала, что немеченый инсулин конкурирует с меченым за связывание с антителами и вытесняет его из иммунных комплексов. Впоследствии Berson и Yalow разработали первый метод РИА для измерения концентрации инсулина в сыворотке, за что они были удостоены Нобелевской премии. В этом методе инсулин, связанный с антителами, отделяли от несвязанного инсулина путем электрофореза на бумаге. Примерно в то же время, в 1960-х гг., Grodsky и Forsham описали сходный метод РИА с использованием 131I-инсулина, но для разделения связанного и несвязанного гормонов они вместо электрофореза применяли высаливание.
Огромный вклад в развитие РИА внесли Hales и Randle в 1963 г. Для разделения связанного и несвязанного гормонов они применили антитела против у-глобулинов, так называемые вторичные антитела. Этот подход основывался на результатах работ Skom и Talmadge, которые в 1958 г. показали, что вторичные антитела вызывают преципитацию комплексов «антиген—первичное антитело». Метод Hales и Randle, получивший название «метода двойных антител», оказался значительно более чувствительным и специфичным, чем прежние варианты РИА.
В 1963 г. Herbert et al. разработали методику отделения комплексов «антиген—антитело» от несвязанного антигена при помощи активированного угля, покрытого декстраном. В основе методики лежит свойство угольно-декстрановой смеси практически мгновенно абсорбировать свободный антиген, не связывая при этом комплексы антиген-антитело. Эта методика позволяет отделять иммунные комплексы гораздо быст7 рее, чем преципитационные методики, поэтому в ней можно использовать 131I-антигены с низкой удельной активностью, меченные по Hunter и Greenwood.
В то же самое время Utiger et al. расширили область применения РИА, разработав способ количественного определения человеческого СТГ. Позднее Greenwood et al. внедрили методику йодирования СТГ, позволяющую получать меченый гормон с удельной активностью 200— 500 мКи/мг (6000-9000 Ки/ммоль).
Эта методика используется и поныне. Суть ее заключается в том, что изотоп йода (1311 или 1251) в составе йодида натрия окисляется хлорамином Т и в таком виде замещает один или несколько атомов водорода в фенольном кольце тирозина и в имидазольном кольце гистидина. Через 1 мин к реакционной смеси добавляют восстановитель, чтобы избежать излишнего повреждения гормона. Отметим, что принцип окислительного йодирования белков был описан Hughes еще в 1957 г. В дальнейшем Meyer и Knobil разработали РИА для измерения человеческого и обезьяньего СТГ, в котором для отделения несвязанного гормона применялся активированный уголь.
Первый РИА для измерения уровня гонадотропных гормонов (в данном случае — ЛГ), разработанный в 1966 г., основывался на использовании антител к человеческому ХГ, поскольку ранее было показано, что эти антитела связываются и с человеческим ЛГ. Один из экспериментов в этой области произвел настоящую революцию в иммунохимии: Catt et al. обнаружили, что антитела способны прилипать к дискам из диазотированного полистирола. Таким образом, отпала необходимость в отделении комплексов антиген—антитело с помощью преципитации или абсорбции. Позднее Catt et al. научились иммобилизировать антитела непосредственно на ненасыщенном полистироле в щелочной среде. Результаты этих работ послужили основой для создания ИФА (см. ниже). Faiman и Ryan впервые сумели получить антисыворотку к гипофизарному гонадотропину — человеческому ЛГ. В дальнейшем были разработаны РИА для определения крысиного ЛГ.
Разработка РИА для измерения уровня ФСГ, как и в случае с ЛГ, начиналась с прицелом на будущие клинические исследования. В 1967 и 1968 гг. несколько научных групп сообщили о новых методах РИА для разных форм человеческого ФСГ. Все они были основаны на методе двойных антител.
В 1967 г. Aria и Lee впервые объявили о способе определения пролактина, основанного на методе двойных антител. Первые измерения уровня пролактина методом РИА были проведены, за отсутствием человеческого материала, в овечьей и бычьей плазме.
Теоретические основы РИА
Первые методы РИА (например, методы Berson и Yalow или Grodsky и Forsham) были основаны на феномене конкурентного ингибирования. Этот феномен заключается в том, что связывание меченого изотопом гормона (меченого антигена) со специфическими антителами подавляется в присутствии немеченого гормона (немеченого антигена). Феномен конкурентного ингибирования можно описать двумя уравнениями: «меченый антиген + антитело меченый комплекс» и «немеченый антиген + антитело <-> немеченый комплекс». Таким образом, число молекул меченого гормона, входящих в состав комплексов антиген—антитело, обратно пропорционально исходному числу молекул немеченого гормона в реакционной смеси. Иначе говоря, радиоактивность комплексов, отделенных от несвязавшихся антител и антигенов, будет тем выше, чем ниже была концентрация немеченого гормона.
Обычно РИА проводят при температуре 4 или 37°С в фосфатно-солевом буферном растворе при рН 7 или 8. Реакция может длиться от 2 до 24 ч (в зависимости от аффинности антител и желаемого уровня чувствительности). Отметим, что автоматизация анализа и усовершенствование способов получения антител значительно сократили время реакции. Когда в реакционной смеси устанавливается равновесие, комплексы антиген—антитело отделяют преципитацией с помощью вторичных антител, абсорбцией свободных антигенов и антител на активированном угле, или осаждением в среде с высокой плотностью, например в среде с полиэтиленгликолем. Если же это твердофазный РИА, то инкубационную среду просто удаляют, а комплексы антиген—антитело остаются на полистироле или другой твердой фазе. На последнем этапе измеряют радиоактивность комплексов. Если гормон был помечен 125I или 131I, используют счетчик у-излучения, если меткой служил 3Н, используют сцинтилляционный счетчик β-частиц. Концентрации гормона в пробах рассчитывают по калибровочной кривой, построенной по результатам измерений в стандартных образцах с известными концентрациями гормона.
Получение антител
Поликлональные антитела для РИА получают путем иммунизации антигеном (гормоном) животных разных видов, в том числе кроликов, кур, морских свинок, уток, коз и овец. Для получения первичных антител (против гормона) обычно используют кроликов и морских свинок, для получения вторичных антител (против первичных) — овец и коз.
Существует множество методов иммунизации, самый распространенный — инъекция антигена в подушечку лапы, или в регионарный лимфоузел, или в селезенку. Так как в организме хозяина антигены существуют очень недолго, для надежной индукции иммунного ответа используют адъювант Фрейнда. Неиммуногенные антигены с небольшой молекулярной массой (например, стероидные гормоны) и антигены с низкой иммуногенностью перед иммунизацией присоединяют к крупным молекулам или частицам (метилированному альбумину, ферритину, декстрану, сефадексу и т. п.). Обычно иммунизацию проводят в несколько этапов с интервалами в 2 недели. Как правило, после нескольких инъекций титр антител в сыворотке быстро растет. Кровь для получения иммунной сыворотки берут из полостей сердца или из вен и артерий уха. Последний способ чаще всего применяют у кроликов. Полученную сыворотку инкубируют 30 мин при 57°С для разрушения комплемента. Затем к сыворотке добавляют консервант, предотвращающий рост бактерий и грибов (азид натрия или тиомерсал).
Моноклональные антитела
В 1975 г. Kohler и Milstein разработали принципиально новую — гибридомную — технологию получения антител. Позже эта разработка была отмечена Нобелевской премией. Опишем основные элементы этой технологии.
Мышей или крыс иммунизируют антигеном, например гормоном. Когда титр антител в сыворотке становится достаточно высоким, у иммунных животных из селе зенки выделяют плазматические клетки среди которых есть и клетки — продуценты антител к исходному антигену. Плазматические клетки гибридизуют in vitro клетками миеломы, происходящими о животных того же вида. Затем клеточную суспензию переносят в селективную среду, в которой выживают только гибридные клетки, а плазматические и миелом ные клетки погибают. Гибридные клети по одной рассевают в лунки с питатель ной средой, где они делятся и образую гибридомы (бессмертные клеточные линии). Среди множества гибридом отбирают те, которые продуцируют антитела нужному антигену, и размножают их питательной среде либо в брюшной полости сингенных мышей. Из питательно; среды или асцитической жидкости выделяют антитела. Эти антитела называют моноклональными, поскольку они продуцируются гибридомой, являющейся потомком одной-единственной плазматической клетки. Моноклональные антитела, вырабатываемые одной гибридомой, распознают только одну детерминанту какого-либо антигена. В этом и состоит принципиальное отличие моноклональных антител от поликлональной антисыворотки, в которой обычно содержится несколько разных антител к различным детерминантам одного антигена.
Одно из важных преимуществ моноклональных антител перед поликлональными заключается в том, что один и тот же вид моноклональных антител с определенной специфичностью и аффинностью можно получать в любых количествах и практически бесконечно (поскольку гибридома бессмертна). Напротив, антительный состав поликлональных антисывороток весьма изменчив, что требует проверки каждой новой партии антисыворотки и подбора условий ее применения. Таким образом, использование моноклональных антител существенно облегчает стандартизацию РИА и других иммунохимических методов анализа.
Получение гормонов, меченных радиоактивными изотопами
Как уже говорилось, для йодирования белковых гормонов чаще всего применяют метод, предложенный Greenwood и Hunter. Изначально в качестве метки использовали 131I, но из-за короткого периода полураспада этого изотопа (8 сут) срок годности меченого гормона был невелик. В 1967 г. Wilde et al. применили для йодирования 125I (Т1/2 = 60 сут). С тех пор этот изотоп применяется для мечения любых белковых и некоторых небелковых гормонов. При этом получаются меченые гормоны с удельной активностью 100—250 мКи/мг. Этого вполне достаточно для надежной регистрации излучения на счетчике ϒ-частиц.
Для мечения небелковых гормонов используют и другие радиоактивные изотопы, такие как излучатели β-частиц 3H или 14C. Меченные 3H или 14C стероиды применяют не только в иммунохимическом анализе гормонов, но и в фундаментальных эндокринологических исследованиях, например для изучения локализации рецепторов стероидов в разных клетках и тканях экспериментальных животных.
Источник

