Анализ крови норма у свиней
| Биохимические показатели | Ед. изм. | Свиноматки | Поросята | |
| Новорожден-ные до кормления | 4-6 дни жизни | |||
| Сыворотки крови Белок общий | г% | 7,5-8,5 | 2,5-3,5 | 5,2-6,3 |
| Гамма-глобулин | г% | 1,8-2,5 | 0-0,32 | 1,0-1,2 |
| Альбумины | г% | 3,0-3,4 | ||
| Кальций общий | мг% | 10-12 | 10-13 | 10-13 |
| Фосфор неорганический | мг% | 5,0-7,0 | 5,0-9,5 | 5,0-8,0 |
| Мочевина | мг% | 30,0-40,0 | ||
| Активность щелочной фосфатазы | ед. Бод. | 1,0-2,0 | 3,0-15 | 3,0-15 |
| Витамин А | мкг% | 20-40 | 10-40 | 10-80 |
| Витамин Е | мг% | 0,25-0,70 | 0,25-1,2 | 0,25-1,2 |
| Витамин В3 | мкг% | 70-85 | 44-70 | |
| Витамин С | мг% | 0,5-0,7 | 0,2-1,0 | 0,2-1,0 |
| Витамин В12 | ммкг/мл | 0,2-0,4 | ||
| Железо в сыворотке | мкг% | 160,0-200,0 | ||
| Йод (СБЙ) | мкг% | 4,0-6,0 | ||
| Цельная кровь Гемоглобин | г% | 10-12 | 8-10 | 8-12 |
| Эритроциты | млн/мкл | 5,0-6,0 | 4,5-6,5 | 4,5-6,5 |
| Гематокрит | 38-46 | 30-46 | 30-46 | |
| Скорость оседания эритроцитов (СОЭ) | мм/час | 15,0-25,0 | ||
| Лейкоциты | тыс/мкл | 12-16 | 8-12 | 10-15 |
| Кетоновые тела | мг% | 1,0-2,0 | ||
| Витамин В12 | мкг% | 10-15 | 10-25 | 10-12 |
| Витамин В2 | мкг% | 5,0-10,0 | 5,0-20,0 | 5-25 |
| Глюкоза | мг% | 60-80 | 80-120 | 80-120 |
| Фосфор неорганический | мг% | 5,0-7,0 | ||
| Медь | мкг% | 80-100 | 110-140 | 70-100 |
| Цинк | мкг% | 200-300 | 110-140 | 100-150 |
| Марганец | мкг% | 10-20 | 10-16 | 12-18 |
| Кобальт | мкг% | 4,0-6,0 | 5-8,5 | 2,3-5,3 |
| Магний | мг% | 3,4,0 | ||
| Печень Витамин А | мг% | 4,0-15,0 | 0,6-0,9 | 0,4-1,2 |
Справочное приложение № 2
Оптимальные параметры микроклимата для свиней.
| № пп | Параметры микроклимата | Свино-матки первого периода супорос-ности и холос-тые | Свино-матки второго периода супорос-ности | Свино-матки подсос-ные | Порося-та-отъемы-шы | Свиньи на откорме |
| 1. | Температура, 0С | |||||
| 2. | Относительная влажность, % | |||||
| 3. | Скорость движения воздуха, м/сек: В холодный и переходный период года | 0,3 | 0,15 | 0,15 | 0,2 | 0,3 |
| В теплый период года | 1,0 | 1,0 | 0,4 | 0,6 | 1,0 | |
| 4. | Концентрация вредных газов: Углекислого газа, % | 0,2 | 0,2 | 0,2 | 0,2 | 0,2 |
| Аммиака, мг/м3 | ||||||
| 5. | Естественная освещенность, ед. КГО | 1,2 | 1,2 | 1,2 | 1,2 | 0,5 |
| 6. | Отношение площади остекления к площади пола | 1:10 | 1:10 | 1:10 | 1:10 | 1:20 |
| 7. | Искусственная освещенность в зоне размещения животных, люкс | 50-100 | 50-100 | 50-100 | 50-100 | 30-60 |
Справочное приложение № 3
Мероприятия по диагностике и профилактике паразитарных заболеваний.
1. Кишечные нематодозы.
Диагноз на кишечные нематодозы ставят на основании микроскопического исследования фекалий и посмертно при обнаружении взрослых гельминтов в кишечнике или их личинок (аскарид – в легких и печени, эзофагостом и трихоцефал в соскобах слизистой оболочки ободочной и слепой кишки соответственно).
Для обнаружения яиц гельминтов в фекальных массах применяют насыщенные растворы аммиачной селитры и плотностью 1,3, поваренной соли 1,2. Личинки аскарид из легочной и печеночной ткани выделяют по Берману.
Гельминтокопрологическому исследованию на кишечные нематодозы подлежат животные не моложе 2,5-3-месячного возраста в количестве не менее 10 % от имеющегося поголовья.
Эффективность дегельминтизации проверяют через 10 дней после ее проведения.
Для дегельминтизации применяют фенбендазол (в лекарственной форме 22,2 % панакура гранулята, 22 % фенкура) в дозе 0,005 г/кг массы животного в течение трех дней подряд групповым способом с кормами или в дозе 0,030 г/кг однократно, а также в дозе 0,015 г/кг в течение двух дней; мебендазол в дозе 0,0066 г/кг живой массы в течение трех дней подряд; ринтал – в дозе 0,005 г/кг однократно, ивермектин в дозе 0,0001 г/кг в течение двух дней.
Для повышения эффективности дегельминтизации наряду с антигельминтиками следует применять иммуностимуляторы (градекс в дозе 0,1 мг/кг, фумаровая кислота в дозе 0,1 г/кг).
Химиопрофилактику необходимо проводить в связи с тем, что поросята-сосуны заражаются кишечными нематодами с первых дней жизни. Раннюю химиопрофилактику проводят, применяя поросятам с 2-недельного возраста ежедневно в течение 45 дней групповым способом с кормами пиперазина адипината в дозе 0,12 г/кг. 20 %-ный тетрамизол гранулят в дозе 0,004 г/кг; фенбендазол один раз в неделю в дозе 0,001 г/кг или мебендазол в дозе 0,002 г/кг, а также ринтал в дозе 0,002 г/кг массы тела до отъема.
Высокоэффективным химиопрофилактическим действием обладает ивермектин, применяемый супоросным свиноматкам за неделю до опороса в дозе 0,0003 г/кг с кормом и через три недели после опороса в такой же дозе.
Оллуланоз.
Прижизненный диагноз ставят путем микроскопии рвотных масс больного животного, а посмертно – путем исследования соскобов со слизистой оболочки желудка в области фульдальных желез. Исследование соскобов проводят с использованием компрессория на трихинеллоскопе, трихинном микропроекторе или под микроскопом с предварительным перевариванием проб в искусственном желудочном соке по методу Ф.А. Волкова (1980) и осаждением гельминтов.
Для лечения применяют:
— ивомек в дозе 1 мл на 33 кг массы тела подкожно однократно;
— ринтал в дозе 5-10 мг/кг массы тела с кормом групповым способом однократно (по АДВ);
— пирантел в дозе 25 мг/кг массы тела с кормом групповым способом два раза в день (по АДВ);
— фенкур в дозе 15 мг/кг массы тела с кормом групповым способом однократно (по АДВ).
Смешанные паразитозы.
Для диагностики смешанных паразитозов свиней необходимо проводить комплексные исследования на гельминтозы и протозоозы. На гельминтозы (аскаридоз, эзофагостомоз, трихоцефалез, стронгилоидоз и др. нематодозы), а также на кокцидиоз диагностические исследования проводить по методу Г.А. Котельникова и В.М. Хренова (1974), на балантидиоз – методом нативного мазка и количественным методом по Н. Манжосу (1982). Гельминтокопроскопические исследования проводят на гельминтозы (аскаридоз, трихоцефалез, эзофагостомоз) через 50-60 дней после предполагаемого заражения, на стронгилятоз – через 8-10 дней, на кокцидиоз через 2-3 недели, на балантидиоз – через 1-2- недели.
Для профилактики паразитозов хряков обследуют на гельминтозы и протозоозы не реже 2 раза в год и при необходимости проводят лечебные мероприятия. В репродукторных, племенных и репродукторно-откормочных хозяйствах свиноматок обследуют на паразитозы и за месяц до опороса проводят химиотерапию с проверкой ее эффективности через 10 дней. При отсутствии возможности осуществлять преимагинальные дегельминтизации, поросят начинают обследовать и дегельминтизировать по достижении 2,5-3-месячного возраста.
Для профилактики смешанных паразитозов свиней используют антигельминтики широкого спектра действия: фенбендазол (в форме 22,2 % панакура или 22 % фенкур) в дозе 0,015 г/кг (по АДВ) два раза подряд; ринтал, мебенвет гранулят 10 %, ивермектин и др. в сочетании с фармазином в дозе 0,02 г/кг массы 2 раза в день в течение 3 дней или сочетание сульгина и сульфадимезина соответственно в дозах 0,075 г/кг и 0,04 г/кг массы в течение 4 дней; трихопол назначают поросятам весом 5-40 кг в дозе 0,25 г, свыше 40 кг – 0,5 г 2 раза в сутки в течение 3 дней; ампролиум в дозе 0,025-0,065 г/кг массы животного два раза в день три-четыре дня подряд и др.
Криптоспоридиоз.
Диагноз ставят на основании обнаружения ооцист криптоспоридий в фекалиях (методом нативного мазка и флотационные методы). Ооцисты выявляют в мазках после окрашивания из по Циль-Нильсену с докрашиванием 1%-ным бриллиантовым зеленым на 100 спирте, по Циль-Габбету, по Козлову.
Обследуют поросят с 3-4-дневного возраста, у павших поросят берут соскобы слизистой оболочки нижней части подвздошной кишки.
Для лечения криптоспоридиоза применяют перорально сульфадимезин в дозе 0,05 г/кг два раза в день и фумаровую кислоту в дозе 0,1 г/кг однократно в течение 5 дней, сульфадимезин в дозе 0,05 г/кг и ампролиум в дозе 0,2 г/кг два раза в день в течение 5 дней.
ПРИЛОЖЕНИЕ 6
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
ПО ЭПИЗООТОЛОГИЧЕСКОМУ ОБСЛЕДОВАНИЮ
Рекомендуемые страницы:
Воспользуйтесь поиском по сайту:
©2015- 2020 megalektsii.ru Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав.
Источник
Показатели | 1 | 1 | 2 | Взрос. |
Гемоглобин, | 91…103 | 86…105 | 89 …93 | 99.. 119 |
Эритроциты, | 4.5…5.5 | 3.8…6.8 | 5.1 …6.8 | 6.0 |
Лейкоциты, * | 5…13 | 5 …17 | 13 …15 | 8 …16 |
Общий | 31…60 | 62 | 56 …75 | 70 …85 |
Альбум., | 12 | 47 ….60 | 35 …37 | 34 ..60 |
Глобул., | 63…70 | 29.5 | 65.1 | 47 …67 |
альфа,% | 14…21 | 12 …24 | 27 | 14 …21 |
бета, | 19…35 | 11 …19 | 0.8 …0.9 | 15 …23 |
гамма,% | 32…50 | 7.0 …8.0 | 23.6 | 15 …23 |
Глюкоза, | 98…100 | 102 | 70 …85 | 80 …100 |
Кальций, | 9.1 | 13.4 …15 | 10.6 | 10 …14 |
Неорг. | 5.2…5.4 | 6 …8 | 6.9 …7.0 | 4 …6 |
По
данным: Васильева Е.А., 1982,
Воскобойник
В.Ф., 1991 и др.
Табл.17
Нормативные
показатели крови у лошадей
Показатели | до | 2 | 4 |
Йод, | 4.48…5.9 | 4.48…5.9 | 2…4 |
Медь, | 33.1…45.8 | 33.1…45.8 | 35…45 |
Кобальт, | 12…13.8 | 12…13.8 | 2.5…5 |
Общий | 63 | 62.5 | 70…78 |
Альбум., | 2.5 | 2.8…3.3 | 3.5…4.5 |
Глобул., | 3.19 | 3.0…3.8 | 3.0 |
Калий, | 14.8…35.3 | 14.8…35.3 | 19…22 |
Мочевина, | 18.6…19.6 | 21…24.5 | 20…36 |
Глюкоза, | 90…104 | 74…86 | 75…95 |
Кальций, | 13.5..14.9 | 13…13.2 | 10…14 |
Неорг. | 4.4…5.2 | 4.4 | 4.2…5.5 |
По
данным: Васильева Е.А., 1982,
Воскобойник В.Ф.,
1991 и др.
Крупный рогатый скот
1. Возрастные группы
Новорожденные
телята
до 1,5 недель
Молочные
телята
от 14 дн. до
3 мес.
Молодняк
3
мес. — 2 года
Случной
возраст
18 мес.
— 2,5 года
Волы
и коровы
после 3
лет
Быки-производители
после 3 лет

Рис.
21. Корова
Определение
возраста
А) по зубам:
1. Шесть
или все молочные зубы, большей частью
покрытые десной, резцы имеют вид
черепичной крыши —
при рождении.
2. Десна
оттягивается с передних резцов. Исчезают
красные ободки —
3 недели.
3.
Черепичный порядок молочных резцов
более не наблюдается. Становится заметным
второй ободок —
1 месяц.
4.
Имеются все молочные резцы, премоляры
и моляры. — 3 месяца.
5. Длина
рогов 10 см — 1 год.
6.
Выпадение первых молочных резцов; рога
до 17 см. – 1.5 года.
7.
Выпадение коренных резцов – 2.3
года.
8.
Имеются коренные резцы – 2.5
года
9.
Выпадение наружных резцов – 2.8
года
10.
Замена наружных резцов – 3—3.5
года
11.
Выпадение молочных клыков – 3.5
года
12.
Смена клыков – 4 года
13.
Половина язычной поверхности зубов
приобретает вид терки – 6
лет
13. Вся
язычная поверхность резцов приобретает
вид терки – 9 лет
14.
Четырехугольная трущая поверхность
на резцах – 10 лет
15.
Видны шейки зубов – 13
лет
16.
Трущая поверхность зубов становится
овальной, появляются пространства
между зубами – 15 лет
17.
Видны только стертые корни — 18-20
лет

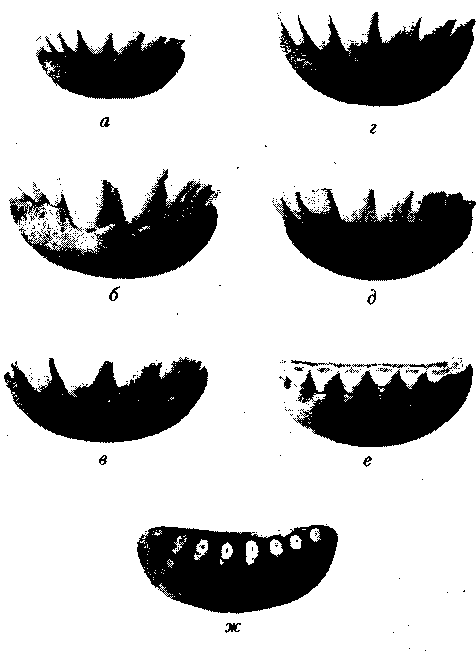
Рис
22. Резцы крупного рогатого скота в семи
возрастных категориях:
а —
около полугода; имеются
молочные резцы; б —
около 2 лет; имеются остатки молочных
резцов (снаружи от коренных); в
— около 2.5 лет; г — около
3 лет; д —
около 4 лет; е — около
14 лет; коронки сильно изношены, видны
шейки зубов; ж — около
18 лет; остаются только корни зубов
(пеньки).
б)
по роговым кольцам:
1 кольцо (после
первого отела) — 2.5…3 года
Появление
следующих колец — после каждого отела
При
яловости расстояние между кольцами
увеличено.
Этот вид определения
возраста не надежен, в отличие от
определения по зубам, т.к. роговые кольца
могут возникать после тяжелой болезни
или бескормицы.
2.
Ректальная температура
Телята от 1 до 14
дней 38,5 — 40,5°С ср.39,5°С
Молодняк
до года
38,5 — 40,0°С
ср.39,2°С
Скот
старше 1 года
37,5 — 39,5°С
ср.38,8°С
Соседние файлы в предмете Физиология животных
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
THE INFLUENCE OF GLUTANIC ACID ON MORPHOLOGICAL AND BIOCHEMICAL BLOOD INDICATORS OF PIGS
Aleksey Karunskiy
professor, the Doctor of Agricultural Sciences Head of the department of genetics, breeding and feeding farm animals
Odessa State Agrarian University,
Ukraine, Odessa
Yanina Rybachenko
a graduate student of the Odessa State Agrarian University,
Ukraine, Odessa
АННОТАЦИЯ
В данной статье рассмотрено влияние добавки глутаминовой кислоты к основному рациону. Установлено, что количество эритроцитов в крови свиней уменьшилось, а лейкоцитов – увеличилось, хотя эти показатели не выходили за границы физиологической нормы. В биохимических показателях крови свиней под влиянием исследуемого фактора отмечено уменьшение альбуминов и β-глобулинов и повышение содержания α-глобулиновых и γ-глобулиновых фракций белка.
ABSTRACT
In this article we examine the influence of glutamic acid additive to the main ration and it was found that the number of red blood cells in the blood of pigs decreased and white blood cells – increased, although these indicators do not go beyond the limits of physiological norm. The blood biochemical parameters of pigs indicated the decrease of albumin and β-globulins, and the increase of α-globulin and γ-globulin protein fractions under the influence of the factor under study.
Ключевые слова: глутаминовая кислота; баланс азота; заменимые аминокислоты; синтетические аминокислоты; откорм свиней.
Keywords: glutamic acid; nitrogen balance; replaceable amino acids; essential amino acids; fattening pigs.
Производство и потребление свинины в мире постоянно растёт. Чтобы получать от свиней качественное и полезное мясо в оптимальные сроки, необходимо их правильно кормить. Свиньи – моногастричные животные, рацион которых должен состоять из быстропереваримых компонентов высокого качества. Известно, что максимальная наследственно обусловленная продуктивность, хорошее здоровье и высокие воспроизводительные способности животных проявляются только в том случае, когда удовлетворяются все их потребности в энергии, аминокислотах, минеральных веществах и витаминах [3, с. 14].
Глутаминовая кислота по химической природе относится к заменимым аминокислотам и входит в состав белков, а также содержится в протеине кормов в свободном состоянии в виде амида (глутамат). Эта кислота всегда присутствует в тканях организма в свободном состоянии и участвует в связывании аммиака, превращаясь при этом в глутамин. Установлено, что в почках и печени под действием фермента глутаминазы глутамин распадается на аммиак и глутаминовую кислоту, которая вновь может быть использована для переноса аммиака из органов и тканей [5, с. 159].
Материалы и методы исследований. Работа была выполнена в ООО «Мрия» Красноокнянского района Одесской области на свиньях крупной белой породы. Было сформировано две группы свиней методом групп-аналогов – контрольная и опытная. Возраст животных от 4 месяцев с одинаковой живой массой 65,6 кг.
Рацион кормления животных составляли два раза в месяц по существующим нормам с учетом возраста и живой массы подопытных свиней. На основе проведенных анализов состава и питательности рационов регулярно осуществляли их сбалансированность по всем 28 показателям. Согласно схеме опыта, животным первой контрольной группы давали рацион без добавления глутаминовой кислоты, а животные второй опытной группы получали рацион, в который добавляли глутаминовую кислоту в количестве 2 г в сутки на 1 голову свиней. Рацион свиней в научно-хозяйственном опыте состоял из следующих кормов (% по питательности): отруби ячменные – 33,0, отруби пшеничные 11,0, отруби гороховые – 17,0, отруби кукурузные – 20,0, силос комбинированный – 12, свекла кормовая – 7. Продолжительность опыта составляла 107 дней. В опыте изучали влияние глутаминовой кислоты на производительность и затраты корма на 1 ц продукции. Схема научно-хозяйственного опыта приведена в таблице 1.
Таблица 1.
Схема научно-хозяйственного опыта
Группа | Количество животных, голов | Продолжительность уравнительного периода | Продолжительность основного периода, дней | Условия кормления |
(ОР) –основной рацион | ||||
(ОР) +2 г Глутаминовой кислоты |
Морфологические и биохимические показатели крови свиней.
Кровь играет важную роль в жизнедеятельности организма. Ее главной функцией является осуществление обмена веществ, который обеспечивает его жизнедеятельность и развитие. Состав крови не постоянен, он изменяется в зависимости от физиологического состояния организма. По картине крови можно определить интенсивность обменных процессов, что дает возможность производить оценку продуктивности животных по косвенным, интерьерным показателям, связанным с величиной селекционных признаков.
Г.В. Максимов, Е.Ю. Гулько подтвердили, что между некоторыми биохимическими, морфологическими показателями крови и мясной продуктивностью существуют тесные взаимосвязи, что указывает на возможность раннего прогнозирования мясной продукции [4, с. 42]. Морфологические показатели крови приведены в таблице 2.
Таблица 2.
Морфологические показатели крови подопытных свиней в научно-хозяйственном опыте
Группа | Норма | ||
1 – контрольная | 2 – опытная | ||
Лейкоцити, тыс./мм3 | 9,85±1,1 | 11,2±1,0 | 8–14 |
Лейкоцитарная формула: | |||
лимфоциты, % | 68,2±4,4 | 65,2±3,6 | 35–45 |
эозинофилы, % | 7,0±1,2 | 6,7±1,75 | 0–4 |
палочкоядерные, % | 0,25 | — | 2–4 |
сегментоядерные, % | 24,0±5,3 | 27,7±3,9 | 40–50 |
двухядерные, % | — | 0.25 | — |
моноцити, % | — | 0.5 | 2–5 |
юни, % | 0,5 | — | 0–2 |
Еритроцити, млн./мм3 | 5,2±0,4 | 5,0±0,4 | 6–8 |
Анализируя лейкоцитарную формулу, можно отметить, что в крови животных опытной группы была большая концентрация сегментоядерных нейтрофилов на 15,4 % по сравнению с животными контрольной группы. У свиней второй группы было также несколько больше двухъядерных и моноцитов, а юных и палочкоядерных не было вообще, в отличие от показателей у контрольных животных.
Количество лимфоцитов в крови свиней опытной группы уменьшилась на 3,0 %, а эозинофилов на 0,3 % по сравнению с контрольной группой, хотя эти показатели были выше физиологической нормы в обеих группах животных.
Результаты биохимических исследований крови свидетельствуют о том, что у животных опытной группы содержание общего белка в сыворотке крови увеличился на 0,5 % по сравнению с контролем, но находился в пределах физиологической нормы (табл. 3).
Следует отметить уменьшение концентрации альбуминов у свиней опытной группы на 4,0 % и глобулинов на 2,0 % по сравнению с животными контрольной группы [1, с. 246].
Таблица 3.
Биохимические показатели крови подопытных свиней в научно-хозяйственном опыте
Группа | Норма | ||
1 – контрольная | 2 – опытная | ||
Общий белок, г% | 2,2±0,25 | 7,7±0,09 | 6,5–8,7 |
В том числе: | |||
альбумины, % | 47,2±6,56 | 43,2±4,18 | 40–55 |
α-глобулины, % | 7,0±1,2 | 6,7±1,75 | 14–20 |
β-глобулины, % | 19,7±2,08 | 17,7±0,65 | 16–21 |
γ -глобулины, % | 21,1±3,62 | 23,9±3,6 | 17–25 |
Гемоглобин, г% | 9,8±0,74 | 10,9±0,5 | 8–14 |
Глюкоза, мг% | 34,9±2,5 | 34,3±1,8 | 60–100 |
Резервная щёлочность мг, % | 480±11,55 | 485±9,6 | 460–520 |
Кальций, мг% | 10,8±0,08 | 10,5±0,26 | 10–14 |
Фосфор неорганический, мг% | 3,25±0,14 | 3,25±0,1 | 4–6 |
Концентрация α-глобулиновых и γ-глобулиновых фракций увеличилась соответственно на 3,2 и 2,8 % по отношению к контрольной группе, показатели крови животных как контрольной, так и опытной групп находились в пределах физиологической нормы.
В проведенном опыте прослеживается тенденция связи между увеличением концентрации гемоглобина в крови свиней опытной группы на 1,1 % по сравнению с животными контрольной группы и увеличением среднесуточных приростов.
Таким образом, результаты биохимических исследований показателей крови свиней свидетельствуют о интенсивность обменных процессов в организме подопытных животных и функционирование их здоровья.
В нашем опыте о нарушении обмена углеводов говорить не приходится, так как уровень глюкозы в сыворотке крови был практически одинаковым у животных обеих групп, но был несколько ниже физиологической нормы.
Содержание кальция в крови подопытных животных обеих групп находится в пределах физиологической нормы, а фосфора находилось несколько ниже нормы у животных как в контрольной, так и опытных группах.
Итак, морфологические и биохимические показатели крови подопытных свиней в научно-хозяйственном опыте дают основание утверждать, что добавка глутаминовой кислоты не влияет отрицательно на обменные процессы в организме животных [1, с. 245].
Под влиянием добавки глутаминовой кислоты количество эритроцитов в крови уменьшилась на 4,05 %, а лейкоцитов увеличилось на 14,3 %, хотя эти показатели были в пределах физиологической нормы. В биохимических показателях крови свиней под действием исследуемого фактора отмечено уменьшение альбуминов на 4,0 %, и β-глобулинов на 2,0 %, и повышение содержания α-глобулиновых и γ-глобулиновых фракций белка соответственно на 3,2 и 2,8 %.
Список литературы:
- Бережнюк Н.А. Морфологічні та біохімічні показники крові свиней при згодовуванні добавок глутамінової кислоти: збірник наукових праць ВДСГІ. – Вінниця, 1998. – Вип. 5. – 270 с.
- Бережнюк Н.А., Паладійчук О.Р., Зміни в органах травлення свиней при підгодівлі їх глутаміновою кислотою: збірник наукових праць ВДСГІ. – Вінниця, 1998. – Вип. 5. – 320 с.
- Голушко В. Линкевич А. Рощин С. Нормирование энерго-протеинового питания свиней: Свиноводство. – 2008.– № 3. – 170 с.
- Гулько Е.Ю., Максимов В.Г., Максимов Г.В. Взаимосвязь биохимических показателей крови с мясной продуктивностью свиней Актуальные проблемы производства свинины: Сб. науч. трудов ДонГАУ. – пос. Персиановский, 2001. – 290 с.
- Жеребцов П.И., Солнцев А.И., Вракин В.Ф. Обмен и биосинтез белка: – М.: Колос, 1968. – 159 с.
- Юрченко В.К., Бережнюк Н.А. Вплив добавки глутамінової кислоти на показники якості продуктів забою свиней: Збірник наукових праць ВДСГІ. – Вінниця, 1999. – Вип. 6. – 258 с.
Источник


