Анализ крови ифа цена инвитро
Метод определения
Иммуноферментный анализ (ИФА).
Исследуемый материал
Сыворотка крови
Комбинированное выявление антител к ВИЧ типов 1 и 2 и антигена р24 ВИЧ, качественный тест.
Внимание. При положительных и сомнительных реакциях, срок выдачи результата может быть увеличен до 10-ти рабочих дней. ВИЧ (вирус иммунодефицита человека), вызывающий СПИД (синдром приобретенного иммунодефицита) — принадлежит к семейству ретровирусов. Передается от человека к человеку при использовании загрязненных игл и шприцев для внутривенного введения наркотиков или терапевтических процедур, при сексуальных контактах, как гетеро, так и гомосексуальных. Передача вируса может произойти при переливании инфицированной крови и ее продуктов, донорстве органов или семенной жидкости, у медицинских работников — при ранении инфицированными иглами или инструментами. Заражение ВИЧ возможно путем его передачи от инфицированной матери ребенку (вертикальный путь), хотя современные методы профилактики с применением антиретровирусной терапии, при выполнении всех рекомендаций, позволяют снизить такой риск до минимума.
В патогенезе заболевания основное значение имеет поражение CD4+ лимфоцитов (субпопуляция лимфоцитов, выполняющих важнейшие функции в регуляции и осуществлении иммунного ответа). Попадая в организм человека, ВИЧ поражает CD4+ лимфоциты, макрофаги и некоторые другие типы клеток. Присутствие ВИЧ со временем вызывает нарушение иммунной системы из-за избирательного уничтожения им иммунокомпетентных клеток. Это приводит к снижению иммунитета против вирусных, бактериальных, грибковых, протозойных, паразитарных, опухолевых заболеваний — развитию синдрома приобретенного иммунодефицита (СПИД). В соответствии со статистикой, раннее выявление инфекции и применение современной терапии значительно улучшают показатели выживаемости.
Процесс взаимодействия вируса с клеткой включает ряд стадий: связывание вируса с клеткой, освобождение его от оболочки, проникновение в цитоплазму, синтез ДНК по вирусной РНК, встраивание вирусной ДНК в геном клетки-хозяина. После этого начинается латентная стадия инфекции. В таком состоянии провирусная ДНК может существовать некоторое время, не проявляя активности и не влияя на жизнедеятельность клетки-хозяина. Пока нет экспрессии вирусных белков, нет и иммунного ответа на вирус. Антитела к ВИЧ, характеризующие иммунный ответ организма, появляются после активации вирусной ДНК и начала активного размножения вируса. Длительность латентного периода зависит от ряда факторов, включая и индивидуальные генетические особенности организма.
Антитела к ВИЧ могут появиться, начиная со второй недели после инфицирования; их содержание увеличивается в течение 2-4-х недель и сохраняется на протяжении многих лет. У 90-95% инфицированных они появляются в первые три месяца после заражения, у 5-9% – в период от трех до шести месяцев, у 0,5-1% – в более поздние сроки.
В первые недели инфекции, еще до появления антител к вирусу (т.е. до сероконверсии), в образцах сыворотки или плазмы можно выявить присутствие антигенов ВИЧ, в том числе его капсидного белка р24. Позже, после сероконверсии, он обычно становится недетектируемым.
Комбинированные тест-системы 4-го поколения, к которым относится тест HIV Ag/Ab Combo (Architect, Abbott), выявляют как антитела к ВИЧ 1 и 2 типов, так и антиген р24 ВИЧ, что позволяет проводить раннее обнаружение инфекции. К особым характеристикам применяемого в лаборатории ИНВИТРО скринингового теста для выявления ВИЧ-инфекции стоит отнести высокую специфичность исследования (> 99,5%); 100% чувствительность анализа к антителам, характерным для периода сероконверсии, и чувствительность теста к антигену р24 порядка 18 пг/мл.
Порядок проведения лабораторного обследования на ВИЧ строго регламентирован приказами МЗ РФ и включает в себя этап скринингового (отборочного) исследования наличия антител к ВИЧ иммуноферментными (ИФА) методами, разрешенными к использованию, и этап верификационного (подтверждающего) более развернутого исследования в лаборатории городского центра СПИД. Следует отметить, что даже лучшие скрининговые ИФА-системы не гарантируют 100% специфичности, то есть существует некоторая вероятность получения неспецифических, ложноположительных результатов, связанных с особенностями сыворотки крови пациента. Поэтому положительный результат скринингового ИФА обследования может не подтвердиться в подтверждающих тестах, после чего пациенту выдадут отрицательный или неопределенный результат. При неопределенном результате подтверждающего исследования тестирование следует повторить в динамике через 2-3 недели.
Лабораторная диагностика ВИЧ инфекции у детей, рожденных от ВИЧ-инфицированных матерей, имеет свои особенности. В их крови до 18-ти месяцев с момента рождения могут циркулировать материнские антитела к ВИЧ (класса IgG). Отсутствие антител к ВИЧ у новорожденных не означает, что вирус не проник через плацентарный барьер. Дети ВИЧ-инфицированных матерей подлежат лабораторно-диагностическому обследованию в течение 36-ти месяцев после рождения.
Источник
Метод определения
Иммуноферментный колориметрический метод.
Исследуемый материал
Сыворотка крови
Определение активности комплемента применительно к классическому, альтернативному и лектиновому путям (раздельно) применяют для скрининга врожденного иммунодефицита.
Комплемент был открыт как термолабильный бактерицидный фактор сыворотки. В современном представлении система комплемента – это сложная система белков сыворотки крови, способных к каскадной активации, включенная в механизмы иммунной защиты и удаления из организма чужеродных клеток, микроорганизмов, продуктов клеточной гибели. Комплемент играет важнейшую роль в обеспечении сопротивляемости инфекциям и поддержании гомеостаза. В организме эта система находится под контролем присутствующих в биологических жидкостях или ассоциированных с мембранами регуляторов. Однако она может быть быстро мобилизована и усилена при необходимости немедленной иммунной реакции на патогенное воздействие.
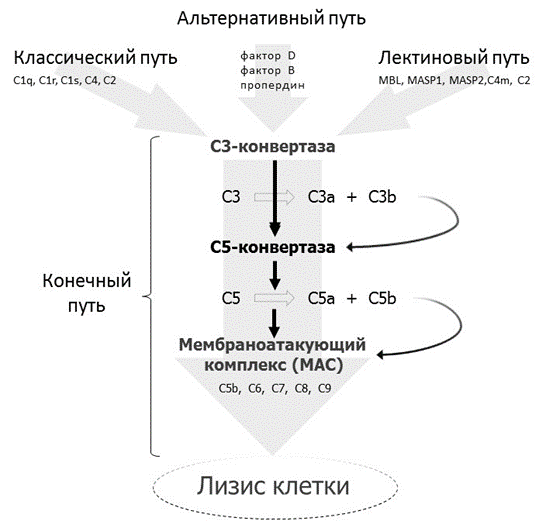
Активация системы комплемента происходит в виде каскадной реакции, которая может осуществляться тремя путями с разными механизмами инициализации (классическим, альтернативным и лектиновым) и общим конечным этапом (Рис.1.). Несоответствующая активация комплемента может вести к хроническому воспалению и повреждению тканей.
Классический путь активации комплемента инициируется комплексами антиген-антитело и агрегированными иммуноглобулинами. Активация альтернативного и лектинового (маннозного) путей не зависит от присутствия антител, индуцируется контактом с определенными структурами бактериальной стенки или иной чужеродной поверхности. Три пути тесно взаимодействуют и сходятся на конечном этапе, что сопровождается формированием опсонинов, анафилотоксинов, хемоаттрактантов и мембраноатакующего комплекса, обеспечивающих эффективный воспалительный и цитолитический ответ на патоген.

Рисунок 1. Схема участия компонентов комплемента в классическом, альтернативном, лектиновом механизмах инициализации и общем конечном пути активации
Каждый из указанных путей активации комплемента может быть задействован не только в механизмах естественной иммунной защиты, но и в патогенезе ряда заболеваний. Дефицит любого из компонентов комплемента приводит к снижению сопротивляемости организма и рецидивирующим инфекциям или несоответствующему воспалительному ответу. Непрерывная патологическая активация комплемента может приводить к повреждению здоровых тканей. Определенные дефекты системы комплемента предрасполагают к развитию аутоиммунной и иммунокомплексной патологии (системной красной волчанки (СКВ), нефритов).
Недостаточность комплемента может быть не только причиной, предрасполагающей к повторным инфекционным заболеваниям и развитию аутоиммунной патологии, но и следствием заболеваний, протекающих с выраженной активацией комплемента. В процессе развития многих инфекционных и аутоиммунных заболеваний происходит повышенное потребление факторов комплемента. Это обнаруживается при лабораторных исследованиях в виде уменьшения концентрации вовлеченных компонентов и снижения функциональной активности соответствующего пути активации комплемента.
Врожденные гомозиготные дефициты компонентов комплемента крайне редки, гетерозиготные (с отсутствием одного аллеля) отмечаются чаще и сопровождаются низким уровнем соответствующих факторов комплемента и снижением его функциональной активности. Приобретенная недостаточность комплемента более распространена. В том числе, как следствие усиленного потребления комплемента в течение иммуновоспалительного процесса или аутоиммунного заболевания.
Предлагаемое исследование комбинирует общие принципы, применяемые в гемолитических методах оценки функции системы комплемента, с использованием иммуноферментного способа распознавания неоантигена мембраноатакующего комплекса, продуцируемого в результате активации системы комплемента. Скрининговое исследование применяется для обследования пациентов при подозрении на врожденный дефицит комплемента либо заболевания, протекающие с потреблением комплемента. С учетом результатов теста дальнейшее обследование пациента при подозрении на врожденный дефицит комплемента может быть нацелено на идентификацию вероятного дефицитного компонента (Таб. 1., раздел «Интерпретация»).
Литература
- Лапин С.В., Тотолян А.А. Иммунологическая лабораторная диагностика аутоиммунных заболеваний. — СПб.: Изд. «Человек». 2010.
- Клиническое руководство Тица по лабораторным тестам (под ред. А. Ву). — М.: Изд. «Лабора». 2013:1280.
- Glovsky M.M. et al. Complement determinations in human disease. Annals of Allergy, Asthma, and Immunology. 2004;93:513-523.
- Nilsson B., Ekdahl K.N. Complement Diagnostics: Concepts, Indications, and Practical Guidelines. Clinical and Developmental Immunology. 2012;2012;11.
- Материалы фирмы-производителя реагентов.
Источник
Хламидиоз — бактериальное инфекционное заболевание системного характера с преимущественно подострым или хроническим течением. Характеризуется поражением эпителия слизистых оболочек (половых органов, глаз, органов дыхательной системы). Инфекция передаётся половым, контактно-бытовым путём.
Группу риска составляют лица, практикующие беспорядочные половые связи и члены семей (особенно дети) инфицированных хламидиозом.
Размеры элементарных телец С. trachomatis очень малы — 0,2 — 0,4 мкм. Это обусловливает неполную защиту половых партнёров механическими средствами контрацепции. Chlamydia trachomatis существует в двух формах: инфекционной (элементарное тельце) — метаболически слабоактивной, приспособленной к существованию во внеклеточной среде, и вегетативной (ретикулярное тельце) — внутриклеточной форме, метаболически активной, образующейся при размножении хламидий. В результате деления ретикулярных телец внутри цитоплазматической вакуоли и их превращения в элементарные тельца формируется до 1000 новых элементарных телец. Цикл развития завершается как правило, гибелью эпителиальной клетки и выходом из нее новых элементарных телец.
При определённых условиях (особенности иммунитета, неадекватная терапия антибиотиками) происходит задержка созревания ретикулярных телец и их превращения в элементарные тельца, что приводит к снижению экспрессии основных антигенов Chlamydia trachomatis, уменьшению иммунного ответа и изменению чувствительности к антибиотикам. Возникает персистирующая инфекция. Реактивация персистирующей инфекции может произойти под действием изменения иммунного или гормонального статуса, травмы, операции, стресса. Интоксикация для хламидийной инфекции не характерна. Исходом воспалительного процесса при хламидиозе является утолщение пораженной слизистой оболочки, метаплазия эпителиоцитов в многослойный плоский эпителий с последующим разрастанием рубцовой соединительной ткани. Последнее, как полагают, является одной из основных причин вторичного бесплодия у мужчин и женщин в результате инфекционного процесса хламидийной этиологии.
Системный характер поражений (в том числе при синдроме Рейтера) имеет аутоиммунный характер и не связан с бактериемией.
Клиническая картина инфекции, в большинстве случаев, не является специфичной. Манифестные формы хламидиоза у мужчин могут протекать в виде уретрита, проктита, конъюнктивита, фарингита. У женщин — уретрита, цервицита, проктита, конъюнктивита, венерической лимфогранулемы. У детей — конъюнктивита, пневмонии, отита, бронхиолита. Наибольшие диагностические трудности представляют бессимптомные формы. Значительные терапевтические проблемы связаны с осложнениями хламидиоза. Это могут быть: сальпингит, эндометрит, внематочная беременность, бесплодие; послеродовый эндометрит, преждевременные роды, невынашивание беременности, мёртворождение, опухоли урогенитального тракта — у женщин; эпидидимит, простатит, синдром Рейтера, бесплодие, ректальные стриктуры — у мужчин.
Хламидиоз: причины, симптомы и диагностика заболевания.
Что такое хламидиоз и как им можно заразиться?
Хламидиоз — одна из самых распространённых инфекций, передающихся половым путём. Ежегодно в мире регистрируют около 90 миллионов новых случаев хламидийной инфекции.
На сегодняшний день хламидиоз занимает первое место в числе наиболее распространённых бактериальных венерических заболеваний в Российской Федерации (учёт ведется с 1993 года). За период 1993 — 2003 гг. распространённость данной инфекции возросла более чем в 3 раза, и с каждым годом этот показатель становится ещё больше. В России ежегодно урогенитальным хламидиозом болеют свыше 1,5 миллиона человек.
Причиной высокой распространённости хламидиоза является то, что многие больные часто не зная, что они могут быть инфицированы, становятся активными распространителями инфекции. И, конечно, не последнюю роль в быстром распространении хламидий играет ведение беспорядочной половой жизни: частая смена половых партнёров без предохранения. При случайных половых связях заболевание обнаруживается у 60% женщин и у 70% мужчин, хотя однократный контакт с больным не всегда приводит к заражению партнёра.
Следует помнить, что половой путь – это не единственный способ заражения. Передаются хламидии и через инфицированные руки, бельё.
Дети могут заразиться хламидиозом во время родов при прохождении через инфицированные родовые пути, а также внутриутробно. В связи с этим очень важно, пройти обследование на хламидии перед запланированной беременностью, и при выявлении – своевременно пройти курс лечения во избежание неприятных последствий для будущего ребенка.
Существует много разновидностей хламидий, но для человека патогенными являются три вида:
- Chlamydophila pneumoniae – инфекция, передающаяся воздушно-капельным путём от инфицированного человека и вызывающая респираторные заболевания;
- Chlamydia pneumonia вызывает пневмонию, которая без специальной терапии может долго персистировать в крови и быть причиной длительного кашля;
- Chlamydophila psittaci (зооантропонозная инфекция) передается от птиц (часто от домашних попугаев и голубей), вызывает заболевание орнитоз — поражение легких. Chlamydia trachomatis — инфекция, передающаяся от человека к человеку и вызывающая трахому (поражение глаз), конъюнктивит и урогенитальные инфекции, венерическую лимфогранулему. Chlamidia trachomatis — в своем роде уникальный микроорганизм, который обитает внутри живой клетки, подобно вирусу, но по своему строению скорее похож на бактерию. Эта двойная природа, а также способность паразитировать внутри клеток и являются причиной того, что выявить и лечить хламидиоз крайне трудно.
Распространённым сопутствующим заболеванием является урогенитальный хламидиоз.
Восприимчивость к урогенитальному хламидиозу приближается к 100%, и особенно высока она у лиц, страдающих иммунодефицитом любого генеза. Наиболее часто урогенитальным хламидиозом болеют мужчины и женщины в сексуально — активном возрасте – 20-40 лет. Также в связи изменением сексуального поведения отмечен рост заболеваемости хламидиозом среди подростков.
Общепринятой клинической классификации урогенитального хламидиоза не существует. Различают свежий и хронический урогенитальный хламидиоз, наблюдают носительство вируса. Свежий — это неосложненный хламидиоз нижних отделов мочеполового тракта. Хронический – это длительно текущий, персистирующий, рецидивирующий хламидиоз верхних отделов мочеполового тракта, включая органы малого таза.
Выделяют ещё восходящую хламидийную инфекцию, т.е. инфекция распространяется по восходящим путям — от нижнего отдела до верхнего отдела мочеполового тракта.
Путей распространения восходящей хламидийной инфекции несколько:
- каналикулярный (через цервикальный канал, полость матки, маточные трубы, на брюшину и органы брюшной полости);
- лимфогенный (по лимфотическим сосудам);
- гематогенный — о нем свидетельствуют экстрагенитальные очаги поражения: (глотка, суставы).
Особенность течения урогенитальной хламидийной инфекции — в отсутствии каких- либо специфических симптомов и выраженной клинической картины с момента инфицирования. Инкубационный период составляет примерно — 2-3 недели.
Несмотря, на то, что патогенез заболевания до конца не изучен, в нем выделяют следующие стадии:
- инфицирование;
- формирование первичного очага инфекции;
- внутриклеточное размножение, ведущее к развитию воспалительного процесса в пораженных клетках и распространению инфекции (эта стадия характеризуется развернутой клинической картиной заболевания);
- органические и функциональные изменения различных органов и систем на фоне развившихся иммунных реакций.
К каким сопутствующим заболеваниям приводит хламидиоз?
Увы, у трети больных хламидийная инфекция протекает совершенно бессимптомно! И за это время человек не только может стать источником заражения, но в его организме ещё и происходят различные осложнения, о которых он порой и не подозревает.
У женщин хламидии могут вызвать уретрит, вестибулит, вагинит, бартоллинит, эндометрит и даже пельвиоперитонит. Кроме того, есть риск развития хламидийного сальпингита (воспаление придатков), вызывающего непрохождение маточных труб и, соответственно, бесплодие.
Хламидиоз может выявляться и у беременных женщин, причем заражение возможно до беременности или во время неё. Наличие данной инфекции у беременных женщин повышает риск угрозы невынашивания, самопроизвольного выкидыша, неразвивающейся беременности, мертворождения, преждевременных родов, несвоевременного излития околоплодных вод, осложнений в родах и послеродовом периоде, а также заражения плода при прохождении через родовые пути.
У мужчин инфицирование хламидиями может привести к уретриту с его непереносимыми частыми позывами к мочеиспусканию, зудом, болью в уретре и гнойными выделениями, простатиту, воспалению яичек (везикулит), эпидидимиту.
Помимо многочисленных осложнений касающихся половых органов, хламидиоз может вызывать поражение других органов и систем: глаз, суставов с развитием реактивных артритов, уретрита.
Какие симптомы возникают при хламидиозе?
Клинические проявления данной инфекции определяют вирулентность (болезнетворность) возбудителя, длительность персистенции хламидий, локализации поражения, выраженность местных и общих реакций организма.
Симптомами острой хламидиозной инфекции являются стекловидные выделения, чаще по утрам, из мочеиспускательного канала, а также возможны боли, рези при мочеиспускании или зуд.
Такие симптомы интоксикации, как слабость и повышение температуры, проявляется в редких случаях. Но чаще всего, хламидиоз протекает бессимптомно. Имеющиеся симптомы могут исчезнуть или периодически проявляться на фоне подавления иммунитета. Таким образом, заболевание приобретает хроническое течение, при этом, возрастает риск поражения все новых систем и органов. Опасность заключается в том, что осложнения, развившиеся вследствие длительного существования инфекции в организме, чаще всего и приводят пациента к врачу.
Как диагностируется хламидиоз?
Очень важное значение при постановке диагноза имеет лабораторная диагностика хламидийной инфекции, поскольку, учитывая чаще всего бессимптомное его течение, только лабораторные методы исследования могут дать верный ответ о наличии хламидиоза в организме.
К самым распространённым и эффективным методом лабораторной диагностики является ПЦР — метод, определяющий специфический участок ДНК хламидий.
Высокая чувствительность ПЦР — метода позволяет выявлять вирус при манифестных, бессимптомных и атипичных клинических формах инфекции, а также и у серонегативных пациентов (когда антитела ещё не определяются) на самых ранних стадиях инфекционного процесса, когда лечение хламидиоза наиболее эффективно.
ПЦР — исследование можно проводить, исследуя и кровь, и выделения из половых путей. Для первичной диагностики, более информативным будет выявление данной инфекции в местах первоначальной локализации, т.е. материалом должны быть выделения из половых путей. У мужчин это может быть как соскоб из уретры, так и исследование эякулята.
Серологический метод исследования — это обнаружение антихламидийных антител в крови. При остром процессе диагностически значимо или обнаружение антител Ig M , или 4-х кратное нарастание титра Ig G в динамике через 2 недели, т.к. иммуноглобулины Ig M образуются в крови сразу после попадания антигенов в организм. Изолированное обнаружение антихламидийных антител не обязательно свидетельствует об инфицированности хламидиозом.
Только одновременное использование двух различных методов, один из которых — ПЦР, дает необходимую точность диагностики хламидиоза и последующего контроля эффективности лечения.
При обнаружении хламидиоза у одного из партнёров (риск заражения партнёра -75-80%) необходимо сдать анализы другим партнёрам, даже в том случае, если у них нет никаких жалоб и симптомов, ведь бессимптомное течение не снижает риска осложнений.
Независимая лаборатория ИНВИТРО предлагает широкий спектр лабораторных исследований, позволяющих выявить хламидиоз на разных стадиях его проявления.
Источник

