Анализ крови аига что это
[13-068]
Антитела к антигенам аутоиммунных заболеваний печени (антитела к микросомам печени-почек 1 типа (LKM-1), пируват-декарбоксилазному комплексу митохондрий (PDC/М2), цитозольному антигену (LC-1) и растворимому антигену печени (SLA/LP)), IgG
3685 руб.
Аутоиммунные заболевания печени относятся к группе заболеваний, при которых в биологических жидкостях обнаруживаются аутоантитела к компонентам клеток и тканей организма человека, которые являются лабораторными диагностическими критериями данных заболеваний.
Синонимы русские
Аутоиммунные заболевания печени.
Синонимы английские
Autoimmune liver diseases.
Метод исследования
Иммуноблотинг.
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Аутоиммунные заболевания печени относятся к группе заболеваний, при которых в биологических жидкостях обнаруживаются аутоантитела, направленные к различным компонентам клеток и тканей организма человека. Существуют три категории аутоиммунных заболеваний печени. Они включают в себя аутоиммунный гепатит, первичные билиарные заболевания печени (первичный билиарный цирроз и первичный склерозирующий холангит) и «перекрестный» синдром. Аутоантитела являются диагностическими лабораторными критериями данных заболеваний.
Аутоиммунный гепатит (АИГ) – это аутоиммунное заболевание печени, проявляющееся слабостью, утомляемостью, мышечными и суставными болями, периодическим повышением температуры тела. Изменения лабораторных данных, характерные для АИГ, включают в себя повышение уровня гамма-глобулинов или иммуноглобулина G (IgG), а также появление в сыворотке крови аутоантител.
Антитела к микросомальной фракции печени и почек (анти-LKM, от англ. anti-liver kidney microsomal) представляют собой гетерогенную группу аутоантител, взаимодействующих с ферментами микросомальной системы окисления печени и почек. Различают несколько вариантов этих антител. Анти-LKM-1 взаимодействуют с ферментом цитохромоксидазой CYP 2D6. Антитела к LKM-1 встречаются у 15 % больных АИГ, в частности у больных АИГ 2-го типа (90 %). Этот вариант аутоиммунного гепатита наиболее характерен для детей, чаще встречается у девочек, чем у мальчиков, и имеет наименее благоприятный прогноз по сравнению с АИГ 1-го и 3-го типов. Также анти-LKM-1 выявляются в сыворотке крови больных (около 5 %) с вирусным гепатитом С. Следует отметить, что обнаружение антител к LKM не является абсолютным диагностическим критерием АИГ, равно как и отрицательный результат на данные аутоантитела не позволяет исключить данный диагноз. Следует проводить комплексное обследование пациентов и исключать все возможные иные причины гепатита. Уровень антител к LKM может снижаться при лечении заболевания, что позволяет использовать этот параметр для оценки активности заболевания.
Антитела к цитозольному антигену 1-го типа (LC-1) и антитела к растворимому антигену печени/поджелудочной железы (SLA/LP) также являются диагностическими маркерами АИГ. Они относятся к лабораторным показателям второй линии диагностики, когда не обнаруживаются антитела первой линии: антитела к гладким мышцам, антинуклеарные антитела и антитела к LKM-1.
Антитела к LC-1 направлены к специфическому метаболическому ферменту печени — формиминотрансферазе циклодеаминазе. Они встречаются у 25-40 % больных при LKM-1-положительном аутоиммунном гепатите 2-го типа. Изолированно анти-LC-1 обнаруживаются в 10 % случаев данного заболевания. Данный тип аутоантител практически не обнаруживается при вирусном гепатите С и АИГ 1-го типа.
Антитела к SLA/LP связываются цитозольным белком-ферментом, содержащим селеноцистеин в пептидных связях (SepSecSбелок), и входят в состав диагностических критериев АИГ. Данные антитела встречаются у 15 % больных АИГ, а также являются лабораторным маркером АИГ в 35 % случаев без обнаружения классических маркеров данного заболевания. Анти-SLA/LP являются высокоспецифичным показателем АИГ 1-го типа, но также редко, до 4 % случаев, выявляются в сыворотке крови больных АИГ 2-го типа, при первичном билиарном циррозе, первичном склерозирующем холангите, целиакии и у здоровых людей.
Антитела к пируват-декарбоксилазному комплексу митохондрий (PDC/М2) отмечаются у 90-95 % больных первичным билиарным циррозом (ПБЦ). Они направлены к пируват-декарбоксилазному комплексу внутренней мембраны митохондрий, который осуществляет расщепление липидов. ПБЦ представляет собой хроническое аутоиммунное заболевание, характеризующееся иммуноопосредованным воспалением и деструкцией малых и средних внутрипеченочных желчных протоков. К симптомам данного заболевания относятся увеличение печени и селезёнки, быстрая утомляемость, слабость, желтуха, зуд кожных покровов. Зачастую первым симптомом является повышение уровня печёночных ферментов, особенно щелочной фосфатазы. Незначительное повышение анти-PDC/М2 может выявляться у пациентов с хроническим активным гепатитом, аутоиммунным гепатитом, у пациентов с другими аутоиммунными заболеваниями, например с системной красной волчанкой, ревматоидным артритом, синдромом Шегрена, системной склеродермией, что указывает на повышенный риск развития первичного билиарного цирроза при этих состояниях.
Современным методом диагностики представленных аутоантител является иммуноблотинг. При данном методе антигенные мишени получают с помощью современных методов молекулярной биологии и генной инженерии, что существенно улучшает диагностические возможности. Метод иммуноблотинга также позволяет одновременно диагностировать несколько аутоантител к конкретным антигенам.
Для чего используется исследование?
- Для диагностики и дифференциальной диагностики аутоиммунных заболеваний печени;
- для диагностики аутоиммунного гепатита 1-го и 2-го типов;
- для диагностики первичного билиарного цирроза;
- для дифференциальной диагностики аутоиммунного гепатита, инфекционных, токсических и наследственных заболеваний печени.
Когда назначается исследование?
- При наличии симптомов острого гепатита: боли в правом подреберье, желтухе кожных покровов и видимых слизистых, лихорадке;
- при наличии симптомов хронического гепатита: слабости, потере веса, анорексии, желтуха в анамнезе, умеренный кожный зуд, кровоточивость десен, носовые кровотечения, артралгии, миалгии;
- при наличии симптомов аутоиммунного гепатита: артралгии, миалгии, умеренные боли в животе, боли в грудной клетке, аменорея, гирсутизм;
- при наличии симптомов первичного билиарного цирроза: утомляемость, слабость, кожный зуд, желтуха, гепатомегалия, спленомегалия, увеличение уровней АЛТ, АСТ, щелочной фосфатазы в сыворотке крови;
- при увеличении активности печеночных ферментов: АЛТ, АСТ, щелочной фосфатазы, гамма-глютамилтранпептидазы;
- при наличии другого аутоиммунного заболевания и подозрении на сочетание нескольких аутоиммунных патологий, наличии «перекрестных» синдромов.
Что означают результаты?
Референсные значения
Компонент | Референсные |
Антитела к Sp-100 | не обнаружены |
Антитела к SLA/LP | не обнаружены |
Антитела к PML | не обнаружены |
Антитела к M2-3E | не обнаружены |
Антитела к микросомам | не обнаружены |
Антитела к LC-1 | не обнаружены |
Антитела к gp210 | не обнаружены |
Антитела к митохондриям | не обнаружены |
Антитела к SS-A (52 кДа) | не обнаружены |
Варианты результата: | |
Причины высокого результата:
- аутоиммунный гепатит 1-го типа;
- аутоиммунный гепатит 2-го типа;
- первичный билиарный цирроз;
- первичный склерозирующий холангит;
- хронический вирусный гепатит С;
- прием некоторых лекарственных препаратов;
- ложноположительный результат при отсутствии признаков поражения печени.
Причины низкого результата:
- отсутствие аутоиммунного заболевания печени или его начальный, серонегативный период;
- ложноотрицателный результат, требующий повторного обследования на уровень аутоантител.
Что может влиять на результат?
- Результат у одного и того же пациента может изменяться в течение болезни, при ее лечении;
- присутствие в сыворотке крови других аутоантител;
- прием лекарственных препаратов.
Важные замечания
- Отсутствие антител к LKM не исключает наличие аутоиммунного гепатита;
- при подозрении на первичный билиарный цирроз наряду с определением АМА необходимо определить уровень активности печеночных ферментов, уровень прямого билирубина и провести биопсию печени.
Также рекомендуется
[13-031] Антитела к гладким мышцам
[13-022] Антитела к микросомальной фракции печени и почек (анти-LKM)
[13-021] Антитела к митохондриям (AMA)
[13-045] Антинуклеарный фактор на HEp-2 клетках
[06-003] Аланинаминотрансфераза (АЛТ)
[06-010] Аспартатаминотрансфераза (АСТ)
[06-013] Гамма-глютамилтранспептидаза (гамма-ГТ)
[06-045] Фосфатаза щелочная общая
[06-037] Билирубин прямой
[30-002] Билирубин непрямой
[06-036] Билирубин общий
Кто назначает исследование?
Терапевт, врач общей практики, гастроэнтеролог, гепатолог, иммунолог, ревматолог, педиатр, инфекционист.
Литература
- Cancado EL, Abrantes-Lemos CP, Terrabuio DRThe importance of autoantibody detection in autoimmune hepatitis / Front Immunol. 2015 May 13;6:222
- Zhang WC, Zhao FR, Chen J, Chen WX Meta-analysis: diagnostic accuracy of antinuclear antibodies, smooth muscle antibodies and antibodies to a soluble liver antigen/liver pancreas in autoimmune hepatitis /PLoS One. 2014 Mar 20;9(3):e92267.
- Yamagiwa S, Kamimura H, Takamura M, Aoyagi Y Autoantibodies in primary biliary cirrhosis: recent progress in research on the pathogenetic and clinical significance /World J Gastroenterol. 2014 Mar 14;20(10):2606-12.
Источник
Что такое аутоиммунная гемолитическая анемия?
Аутоиммунная гемолитическая анемия — это аутоиммунное заболевание, характеризующееся преждевременным разрушением здоровых эритроцитов (клеток крови) аутоантителами.
Аутоиммунные заболевания возникают, когда естественная защита организма от чужеродных организмов (например, лимфоцитов, антител) разрушает здоровые ткани по неизвестным причинам. Обычно эритроциты имеют продолжительность жизни около 120 дней, прежде чем будут удалены селезенкой.
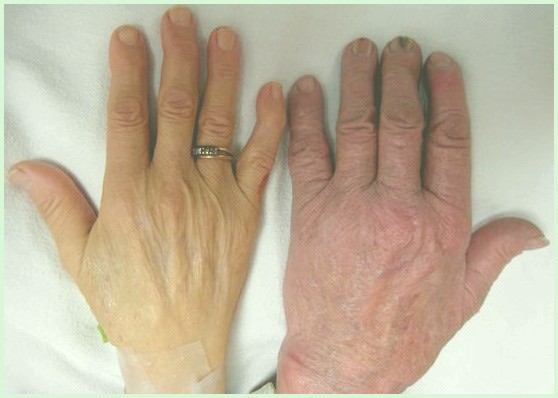
Медицинским термином для низких уровней циркулирующих эритроцитов является анемия. Анемия может вызывать усталость, бледный цвет кожи, пожелтение кожи и белых глаз (желтуха) и отток крови в моче (гемоглобинурия), что придаст моче темно-коричневый цвет.
Признаки и симптомы

Симптомы аутоиммунной гемолитической анемии обычно развиваются медленно в течение периода от нескольких недель до месяцев, но в некоторых случаях могут развиваться внезапно в течение нескольких дней.
Конкретные симптомы, которые возникают, могут варьироваться от одного человека к другому и могут зависеть от скорости возникновения, скорости разрушения здоровых эритроцитов и наличия основного расстройства.
Некоторые люди, особенно те, у кого постепенно развивается анемия, могут не иметь каких-либо явных симптомов. У пострадавших людей могут в конечном итоге развиться:
- ненормальная бледность кожи;
- усталость;
- затрудненное дыхание при физической нагрузке;
- головокружение;
- учащенное сердцебиение.
Желтизна кожи и белых глаз (желтуха) и увеличение селезенки (спленомегалия) также часто встречаются у людей с аутоиммунной гемолитической анемией.
Спленомегалия может привести к тому, что у пострадавшего появится вздутие живота или ощущение полного отека в животе. Иногда у некоторых людей может происходить увеличение печени (гепатомегалия).
У людей с тяжелыми случаями, особенно с быстрым (острым) началом, могут развиться более серьезные осложнения, в том числе потеря сознания (обмороки), боль в груди (стенокардия), аномально быстрое сердцебиение (тахикардия) и сердечная недостаточность.
Причины аутоиммунной гемолитической анемии
Причина аутоиммунной гемолитической анемии обычно неизвестна (т. е. идиопатическая). Однако расстройство может возникать как часть более крупного расстройства, эти случаи известны как вторичная аутоиммунная гемолитическая анемия.
Аутоиммунная гемолитическая анемия является аутоиммунным расстройством — расстройством, при котором естественная защита организма от вторжения организмов (например, лимфоцитов, антител) разрушает здоровые ткани по неизвестным причинам. Антитела ошибочно атакуют здоровые эритроциты, вызывая преждевременное разрушение клеток, состояние, называемое гемолизом.
Антитела (которые также известны как иммуноглобулины) представляют собой специализированные белки, которые связываются с инвазивными организмами и вызывают их разрушение. Существует пять основных классов антител – IgA, IgD, IgE, IgG и IgM.
Большинство случаев данной анемии происходят из-за антител IgG, которые по ошибке атакуют здоровые эритроциты. Реже антитела IgM или IgA вызывают расстройство. Когда антитела атакуют здоровые ткани, их можно назвать аутоантителами.
Несколько основных расстройств связанных с гемолитической анемией, включают другие аутоиммунные расстройства, такие как системная красная волчанка и расстройства, характеризующиеся перепроизводством лейкоцитов (лимфопролиферативные расстройства), такие как лейкемия или лимфома.
Вторичная аутоиммунная гемолитическая анемия также может возникнуть как побочный эффект некоторых лекарств.
Затронутые группы населения
Гемолитическая анемия поражает мужчин и женщин в равных количествах. По оценкам, аутоиммунные гемолитические анемии затрагивают 1-3 человека на 100 000 населения в целом. У людей любого возраста, включая детей, может развиться данная болезнь, однако чаще она встречается у взрослых с пиковой заболеваемостью в возрасте 50-70 лет.
Диагностика
Диагноз гемолитической анемии можно заподозрить на основании тщательной клинической оценки, детальной истории болезни, выявления характерных симптомов и различных анализов, таких как анализы крови, которые измеряют гемоглобин и гематокрит. Гемоглобин — белок в красных кровяных клетках, который переносит кислород. Гематокрит — процент от общего объема крови, занимаемый эритроцитами.
Анализы крови могут также показать повышенный уровень незрелых эритроцитов (ретикулоцитов), который происходит, когда организм вынужден производить дополнительные эритроциты, чтобы восполнить те, которые преждевременно разрушились. Некоторые люди с гемолитической анемией имеют повышенный уровень билирубина в крови (гипербилирубинемия). Билирубин — желтоватый продукт, образующийся при метаболизме гемоглобина в печени.
Когда предполагается, что анемия вызвана дисфункцией иммунной системы (т. е. аутоиммунная гемолитическая анемия), могут проводиться специализированные тесты, такие как проба Кумбса. Этот анализ проводиться для обнаружения антител, которые действуют против эритроцитов. Образец крови берется и затем подвергается воздействию реагента Кумбса. Если эритроциты слипаются в присутствии реагента то, это указывает на наличие у пациента заболевания.
Лечение аутоиммунной гемолитической анемии
Лечение аутоиммунной гемолитической анемии является симптоматическим и поддерживающим. Пострадавших людей обычно лечат кортикостероидными препаратами, такими как преднизон, и обычно они контролируют болезнь при правильном лечении. Первоначально может быть рекомендована высокая доза этих лекарств с последующим постепенным снижением дозы в течение следующих нескольких недель или месяцев.
Людям, которые не отвечают на терапию кортикостероидами или развивают непереносимые побочные эффекты, могут быть назначены иммунодепрессанты или хирургическое удаление селезенки (спленэктомия). Иммуносупрессивные лекарственные средства, такие как циклофосфамид, представляют собой лекарственные средства, которые подавляют или блокируют иммунную систему, и помогают некоторым людям с гемолитической анемией, которые не реагируют на преднизон или спленэктомию.
Спленэктомия обычно используется у людей с тяжелыми случаями, которые требуют постоянного преднизона для контроля. У пациентов с основным нарушением лечение этого расстройства обычно приводит к заметному улучшению анемии.
Ритуксимаб — это моноклональное антитело, искусственно созданное антитело, которое нацелено на определенные лейкоциты, которые создают антитела, которые преждевременно разрушают эритроциты. Ритуксимаб оказался полезным для некоторых пациентов с аутоиммунной гемолитической анемией, которые не реагировали на преднизон. Уровень ответов может достигать 80% у взрослых и 60% у детей. Ритуксимаб может быть использован до спленэктомии или может использоваться у людей, у которых наблюдается рецидив после спленэктомии.
Переливание эритроцитов также может быть необходим для поддержания надлежащего уровня эритроцитов у людей с тяжелыми случаями. Этот поддерживающий метод обеспечивает временное облегчение состояния, но не лечит основную причину расстройства.
Профилактика
Предотвратить аутоиммунную гемолитическую анемию не возможно, но врачи могут помочь людям, у которых есть вирусная инфекция или которые используют определенные лекарства, чтобы болезнь не развивалась.
Тяжелая анемия может усугубить многие проблемы, такие как болезни сердца и легких. Люди должны обратиться к врачу, если они испытывают какие-либо симптомы, которые могут указывать на гемолитическую анемию.
Источник
Иммунолог Надежда Кнауэро патогенезе, клинике и лечении иммунного поражения печени
Аутоиммунный гепатит (АИГ) — это хроническое воспалительное заболевание печени, характеризующееся утратой иммунологической толерантности организма к тканевым антигенам [1, 2].
Впервые сведения о тяжелом поражении печени с выраженной желтухой и гиперпротеинемией появились в 30–40‑х гг. XX века. В 1950 г. шведский врач Ян Вальденстрем (Jan Waldenström) наблюдал у 6 молодых женщин хронический гепатит с желтухой, телеангиоэктазиями, повышением СОЭ, гипергаммаглобулинемией. Гепатит хорошо отвечал на лечение кортикотропином [3]. Из-за сходства лабораторных изменений с картиной системной красной волчанки (наличие антинуклеарных антител в сыворотке, положительные результаты LE-теста) одним из названий патологии стал «люпоидный гепатит».
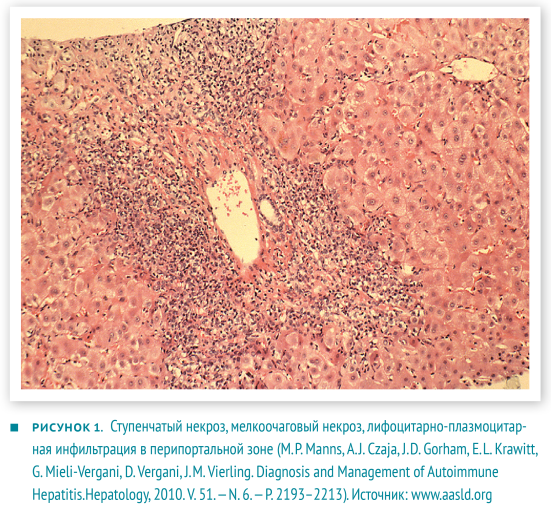
В настоящее время аутоиммунный гепатит определяют как хронический, преимущественно перипортальный гепатит с лимфоцитарно-плазмоцитарной инфильтрацией и ступенчатыми некрозами (рис. 1). Характерные проявления: гипергаммаглобулинемия, появление аутоантител в крови.
Классификация
В зависимости от вида аутоантител выделяют три типа заболевания:
- АИГ 1 типа встречается наиболее часто и характеризуется появлением в крови антинуклеарных антител (АНА, antinuclear antibodies, ANA) и/или антител к гладким мышцам (АГМА, smooth muscle antibodies, SMA).
- При АИГ 2 типа образуются аутоантитела к микросомальным антигенам печени и почек (anti-liver kidney microsomal type-1 antibodies, anti-LKM-1).
- АИГ 3 типа связан с образованием аутоантител к растворимому печеночному антигену, ткани печени и поджелудочной железы (anti-soluble liver antigen/liver-pancreas antibodies, anti-SLA/LP).
Некоторые авторы объединяют АИГ 1 и АИГ 3 в силу сходства клинико-эпидемиологических особенностей [4].Существуют также перекрестные формы (overlap syndrome) различных аутоиммунных патологий печени, включающие в себя АИГ: АИГ+ПБЦ (первичный билиарный цирроз), АИГ+ПСХ (первичный склерозирующий холангит). Пока не вполне ясно, следует ли считать эти заболевания параллельно текущими самостоятельными нозологиями или частями непрерывного патологического процесса.
В качестве отдельной нозологии рассматривается АИГ, развившийся de novo после трансплантации печени, выполненной по поводу печеночной недостаточности, связанной с другими заболеваниями [1, 5].
Аутоиммунный гепатит встречается повсеместно. Распространенность АИГ в европейских странах — около 170 случаев на 1 млн населения. При этом до 80 % всех случаев составляет АИГ 1 типа. АИГ 2 типа распространен неравномерно — до 4 % в США и до 20 % в Европе.
Болеют преимущественно женщины (соотношение полов среди пациентов в странах Европы составляет 3–4:1). Возраст заболевших — от 1 года до 80 лет, средний возраст — около 40 лет [6].
Этиопатогенез
Этиология АИГ неизвестна, однако считается, что на развитие заболевания влияют как генетические факторы, так и факторы окружения.
Важным звеном патогенеза могут быть определенные аллели генов HLA II (человеческий лейкоцитарный антиген типа II, Human leucocyte antigen II) и генов, связанных с регуляцией деятельности иммунной системы [7, 8].
Отдельно стоит сказать об АИГ, входящем в клиническую картину аутоиммунного полиэндокринного синдрома (autoimmune polyendocrine syndrome, autoimmune polyendocrinopathy-candidiasis-ectodermal dystrophy, APECED). Это моногенное заболевание с аутосомно-рецессивным наследованием, связанное с мутацией в гене AIRE1. Таким образом, в данном случае генетическая детерминированность является доказанным фактом [4, 9].
Аутоиммунный процесс при АИГ представляет собой Т-клеточный иммунный ответ, сопровождающийся образованием антител к аутоантигенам и воспалительным повреждением тканей.
Факторы патогенеза АИГ:
- провоспалительные факторы (цитокины), продуцируемые клетками в ходе иммунного ответа. Косвенным подтверждением может служить то, что аутоиммунные заболевания часто бывают сопряжены с бактериальными или вирусными инфекциями;
- угнетение активности регуляторных Т-клеток, играющих важнейшую роль в поддержании толерантности к аутоантигенам;
- нарушение регуляции апоптоза, в норме — механизма, контролирующего иммунный ответ и его «правильность»;
- молекулярная мимикрия — явление, когда иммунный ответ против внешних патогенов может затрагивать и структурно схожие с ними собственные компоненты. Важную роль в этом могут играть вирусные агенты. Так, в нескольких исследованиях было показано наличие пула циркулирующих аутоантител (ANA, SMA, anti-LKM-1) у пациентов, страдающих вирусными гепатитами В и С [2,4];
- фактор токсического лекарственного воздействия на печень. Некоторые исследователи связывают манифестацию АИГ с употреблением противогрибковых препаратов, нестероидных противовоспалительных средств.
Клиника
Примерно у четверти больных АИГ начинается остро, описаны даже редкие случаи развития острой печеночной недостаточности. Острый гепатит с желтухой чаще встречается у детей и молодых людей, у этой же группы чаще отмечается фульминантное течение заболевания [6].
Следует отметить, что у некоторых пациентов с явлениями острого АИГ в отсутствие лечения может наблюдаться спонтанное улучшение состояния и нормализация лабораторных показателей. Однако через несколько месяцев обычно наступает повторный эпизод АИГ. Гистологически также определяется персистирующий воспалительный процесс в печени [6].
Чаще клиника АИГ соответствует клинике хронического гепатита и включает в себя такие симптомы, как астения, тошнота, рвота, боли или дискомфорт в правом верхнем квадранте живота, желтуха, порой сопровождающаяся кожным зудом, артралгии, реже — пальмарная эритема, телеангиэктазии, гепатомегалия [2, 6]. При развившемся циррозе печени могут превалировать симптомы портальной гипертензии, явления энцефалопатии.
АИГ может быть сопряжен с аутоиммунными заболеваниями различных профилей:
- гематологического (тромбоцитопеническая пурпура, аутоиммунная гемолитическая анемия);
- гастроэнтерологического (воспалительные заболевания кишечника);
- ревматологического (ревматоидный артрит, синдром Шегрена, системная склеродермия);
- эндокринного (аутоиммунный тиреоидит, сахарный диабет);
и других профилей (узловая эритема, пролиферативный гломерулонефрит) [1, 2].
Диагностика АИГ
Диагностика аутоиммунного гепатита основывается на:
- результатах исследований: клинического, серологического и иммунологического;
- исключении других заболеваний печени, протекающих с аутоиммунным компонентом или без оного (хронический вирусный гепатит, токсический гепатит, неалкогольный стеатоз, болезнь Вильсона, гемохроматоз, а также криптогенный гепатит).
АИГ 1 и 3 типа схожи по демографическим характеристикам заболевших, профилю HLA, активности воспалительного процесса и ответу на терапию. Существенные отличия имеет АИГ 2 типа, поражающий чаще детей и подростков и обычно имеющий острое начало и более тяжелое течение.
Необходимо помнить о вероятном АИГ у пациентов с повышением уровня печеночных ферментов, а также у пациентов с циррозом печени. При наличии признаков холестаза в круг патологий для проведения дифференциального диагноза следует включить первичный билиарный цирроз и первичный склерозирующий холангит.
Клинический поиск включает в себя определение таких лабораторных показателей, как активность аланинаминотрансферазы и аспартатаминотрансферазы (АЛТ и АСТ), щелочной фосфатазы (ЩФ), уровень альбумина, гамма-глобулина, IgG, билирубина (связанного и несвязанного). Необходимо также определение уровня аутоантител в сыворотке крови и получение данных гистологического исследования [9].
Для больных, у которых в течение 4 лет не удалось достичь ремиссии и приостановить развитие цирроза, метод выбора — трансплантация печени. 10‑летняя выживаемость у пациентов, перенесших эту операцию, достаточно высока (75–85 %), однако и доля рецидивов достигает 11–41 %. Сохранение аутоантител в крови не является признаком рецидива АИГ и не позволяет предсказать его развитие.
Методы визуальной диагностики (УЗИ, КТ, МРТ) не имеют решающего вклада в диагностику АИГ, однако позволяют установить факт прогрессии АИГ и исход в цирроз печени, а также исключить наличие очаговой патологии.В целом диагностика базируется на 4 пунктах [10]:
- Гипергаммаглобулинемия — один из наиболее доступных тестов. Показательно повышение уровня IgG при нормальном уровне IgA и IgM. Однако существуют трудности при работе с пациентами с исходно низким уровнем IgG, а также с пациентами (5–10 %) с нормальным уровнем IgG при АИГ. В целом этот тест считается полезным при мониторинге активности заболевания на фоне лечения [6].
- Наличие аутоантител. При этом антитела типов ANA и SMA не являются специфическим признаком аутоиммунного гепатита, также как и антитела anti-LKM-1, встречающиеся у 1/3 детей и малой части взрослых, страдающих АИГ. Только антитела anti-SLA/LP специфичны для АИГ. Также у пациентов могут определяться антитела к двухцепочечной ДНК.
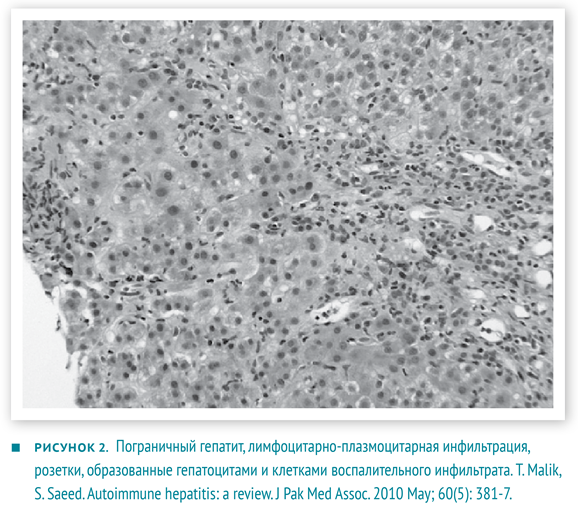
- Гистологические изменения, оцениваются в комплексе с предыдущими показателями. Не существует строго патогномоничных признаков АИГ, но многие изменения являются весьма типичными. Портальные поля инфильтрированы в разной степени Т-лимфоцитами и плазмоцитами. Воспалительные инфильтраты способны «отсекать» и разрушать отдельные гепатоциты, проникая в паренхиму печени, — данное явление описано как ступенчатый (мелкоочаговый некроз), пограничный гепатит (interface hepatitis). Внутри долек возникает баллонная дегенерация гепатоцитов с их отеком, образованием розеток и некрозом отдельных гепатоцитов — рис. 2. Для фульминантного течения часто характерны центролобулярные некрозы. Также могут наблюдаться мостовидные некрозы, соединяющие соседние перипортальные поля [2, 6].
- Отсутствие маркеров вирусного гепатита.
- Международной группой по исследованию АИГ разработана балльная система для оценки достоверности диагноза — табл. 1.
Лечение аутоиммунного гепатита
АИГ относится к заболеваниям, при которых лечение позволяет существенно повысить выживаемость больных.
Показаниями для начала лечения служат:
- повышение активности АСТ в сыворотке крови в 10 раз по сравнению с нормой или в 5 раз, но в сочетании с двукратным повышением уровня гамма-глобулина;
- наличие мостовидных или мультилобулярных некрозов при гистологическом исследовании;
- выраженная клиника — общие симптомы и симптомы поражения печени.
Менее выраженные отклонения в лабораторных показателях в сочетании с менее выраженной клиникой являются относительным показанием к лечению. При неактивном циррозе печени, наличии признаков портальной гипертензии в отсутствие признаков активного гепатита, при «мягком» гепатите со ступенчатыми некрозами и без клинических проявлений лечение не показано [1, 9].
Общая концепция терапии при АИГ предполагает достижение и поддержание ремиссии. Базовой является иммуносупрессивная терапия — глюкокортикостероиды (преднизолон) в качестве монотерапии или в сочетании с азатиоприном [2, 6, 9, 11]. Терапия продолжается до достижения ремиссии, причем важно достичь именно гистологически подтвержденной ремиссии, которая может отставать от нормализации лабораторных показателей на 6–12 мес. Лабораторная же ремиссия описывается как нормализация уровня АСТ, АЛТ, гамма-глобулина, IgG [2].
Поддерживающую терапию более низкими дозами иммуносупрессантов для снижения вероятности рецидива после достижения ремиссии проводят по крайней мере в течение 2 лет.
Кроме того, обсуждается возможность применения препаратов урсодезоксихолевой кислоты (УДХК)при аутоиммунном гепатите в качестве сопутствующей терапии или даже монотерапии [11]. АИГ у пациентов, получавших препараты УДХК при моно- и комбинированной терапии, характеризовался более мягким течением и ускоренной нормализацией лабораторных показателей.
Ответ на лечение
Результаты лечения преднизолоном и азатиоприном при АИГ могут быть следующими:
- Полный ответ — нормализация лабораторных показателей, которая сохраняется в течение года на фоне поддерживающей терапии. При этом нормализуется и гистологическая картина (за исключением небольших остаточных изменений). О полной эффективности лечения говорят и в тех случаях, когда достоверно уменьшается выраженность клинических маркеров аутоиммунного гепатита, и в течение первых месяцев терапии лабораторные показатели улучшаются по крайней мере на 50 % (а в последующие 6 месяцев не превышают нормальный уровень более чем в 2 раза).
- Частичный ответ — отмечается улучшение клинических симптомов и в течение первых 2 месяцев наблюдается улучшение лабораторных показателей на 50 %. В последующем положительная динамика сохраняется, однако полной или практически полной нормализации лабораторных показателей в течение года не происходит.
- Отсутствие терапевтического эффекта (неэффективность лечения) — улучшение лабораторных показателей менее чем на 50 % в первые 4 недели лечения, причем дальнейшего их снижения (вне зависимости от клинического или гистологического улучшения) не происходит.
- Неблагоприятный исход терапии характеризуется дальнейшим ухудшением течения заболевания (хотя в некоторых случаях и отмечается улучшение лабораторных показателей).
О рецидиве заболевания говорят, когда после достижения полного ответа вновь появляются клинические симптомы и ухудшаются лабораторные показатели.
Обычно терапия дает хороший эффект, однако у 10–15 % больных она не приводит к улучшению, хотя и хорошо переносится. Причинами неэффективности терапии могут служить [6]:
- отсутствие ответа на препарат;
- отсутствие комплаенса и приверженности терапии;
- непереносимость препаратов;
- наличие перекрестных синдромов;
- гепатоцеллюлярная карцинома.
В качестве альтернативных препаратов для лечения аутоиммунного гепатита используют и другие иммуносупрессоры: будесонид, циклоспорин, циклофосфамид, микофенолата мофетил, такролимус, метотрексат [1, 2, 6, 11].
Клинический случай
Девочка восьми лет наблюдалась по поводу кожных высыпаний (эритематозные и нодулярные элементы без какого‑либо отделяемого на нижних конечностях), беспокоящих ее в течение 5–6 мес. Два месяца использовала местные средства от экземы, улучшения не было. Позднее возникли дискомфорт в эпигастральной области, слабость, периодически — тошнота и рвота.
Высыпания локализовались на ногах. При гистологическом исследовании кожного биоптата выявлена инфильтрация подкожной жировой клетчатки лимфоцитами без признаков васкулита. Данные явления были расценены как узловатая эритема.При осмотре выявлена невыраженная гепатоспленомегалия, в остальном соматический статус — без выраженных особенностей, состояние стабильное.
По результатам лабораторных исследований:
- ОАК: лейкоциты — 4,5×109/л; нейтрофилов 39 %, лимфоцитов 55 %; признаки гипохромной микроцитарной анемии (гемоглобин 103 г/л); тромбоциты — 174,000/мкл, СОЭ — 24 мм/ч;
- биохимический анализ крови: креатинин — 0,9 мг/дл (норма 0,3–0,7 мг/дл); билирубин общий — 1,6 мг/дл (норма 0,2–1,2 мг/дл), билирубин прямой – 0,4 мг/дл (норма 0,05–0,2 мг/дл); АСТ — 348 Ед/л (норма — до 40 Ед/л), АЛТ — 555 Ед/л (норма — до 40 Ед/л); щелочная фосфатаза — 395 Ед/л (норма — до 664 Ед/л), лактатдегидрогеназа — 612 Ед/л (норма — до 576 Ед/л).
Показатели системы гемостаза (протромбиновое время, международное нормализованное отношение), уровень общего белка, сывороточного альбумина, гамма-глобулина, уровень ферритина, церулоплазмина, альфа-антитрипсина, гамма-глутамилтранспептидазы — в пределах референсных значений.
В сыворотке крови не выявлены HBs-антиген, антитела к HBs, HBc, антитела к вирусу гепатита А и С. Также отрицательными были тесты на цитомегаловирус, вирус Эпштейна — Барр, токсоплазму, бруцеллу. Титр АСЛ-О в пределах нормы.Данных за сахарный диабет, тиреоидит, болезнь Грейвса, пролиферативный гломерулонефрит — не выявлено.
При УЗИ органов брюшной полости визуализировалась увеличенная печень с измененной эх?


